题目内容
4.工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:2FeSO4═Fe2O3+SO2↑+SO3↑ 为检验FeSO4高温分解的产物,进行如下实验:①取少量FeSO4高温分解得到的固体,加一定量稀盐酸溶解,向该溶液中加入适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在.
②将FeSO4高温分解产生的气体通入图所示的装置中,以检验产生的气体中是否含有SO2和SO3.请回答以下问题:

(1)写出用KSCN检验Fe3+的离子方程式Fe3++3SCN-=Fe(SCN)3.
(2)装置I中试剂为氯化钡溶液,进行操作②时氯化钡溶液中有白色沉淀产生.甲同学说,这个白色沉淀可能是BaSO4和BaSO3的混合物;乙同学说,这个白色沉淀是BaSO4;丙同学说,这个白色沉淀是BaSO3.请你设计一个简单的实验帮他们加以鉴别.取Ⅰ中白色沉淀,加入足量稀盐酸,若沉淀不溶解且无气泡产生,则沉淀为BaSO4
你认为上述哪一位同学的观点正确?乙
(3)装置II中试剂为品红溶液,其作用是检验产生的气体中含SO2,品红溶液中可观察到现象是品红溶液褪色.
(4)装置III中试剂为NaOH溶液,其目的是除去多余的SO2,防止污染空气.
分析 (1)铁离子与硫氰根离子结合生成硫氰化铁,据此书写离子方程式;
(2)亚硫酸钡能够溶于盐酸,而硫酸钡不溶于盐酸,用盐酸可以鉴别;
(3)二氧化硫具有漂白性,能够使品红溶液褪色,据此可检验二氧化硫;
(4)二氧化硫有毒,多余的二氧化硫需要用氢氧化钠溶液吸收.
解答 解:(1)KSCN检验Fe3+反应生成硫氰化铁,反应的离子方程式为:Fe3++3SCN-=Fe(SCN)3,
故答案为:Fe3++3SCN-=Fe(SCN)3;
(2)BaSO4不溶于盐酸,而BaSO3溶于盐酸,可用盐酸鉴别二者,操作方法为:取Ⅰ中白色沉淀,加入足量稀盐酸,若沉淀不溶解且无气泡产生,则沉淀为BaSO4;
氯化钡不与二氧化硫反应,生成的沉淀为硫酸钡沉淀,则乙同学说法合理,
故答案为:取Ⅰ中白色沉淀,加入足量稀盐酸,若沉淀不溶解且无气泡产生,则沉淀为BaSO4;乙;
(3)SO2能够使品红溶液褪色,装置II中试剂为品红溶液,若品红溶液褪色,证明生成产物中含有二氧化硫,
故答案为:检验产生的气体中含SO2;品红溶液褪色;
(4)装置III中试剂为NaOH溶液,氢氧化钠溶液能够与二氧化硫反应,避免污染空气,
故答案为:除去多余的SO2,防止污染空气.
点评 本题考查性质方案的设计,题目难度不大,明确实验目的为解答关键,注意熟练掌握常见元素及其化合物性质,试题有利于提高学生的分析能力及化学实验能力.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | PM2.5亦称可入肺颗粒物,表面积相对较大,会吸附有害物质 | |
| B. | 煤的气化和石油的分馏都是物理变化 | |
| C. | 从海水中提取物质都必须通过化学反应才能实现 | |
| D. | “嫦娥”三号使用的碳纤维是一种新型的有机高分子材料 |
5.有4种碳架如下的烃,下列说法正确的是( )


| A. | a和b互为同分异构体 | B. | b和c是同系物 | ||
| C. | a和b都能发生加成反应 | D. | 只有b和c能发生取代反应 |
13.环境污染与资源短缺问题日趋突出,高效循环利用资源显得尤为重要.工业上用含有Cu2O、Al2O3、Fe2O3和SiO2的矿渣提取铜的工艺流程如图:

已知:①Cu2O+2H+=Cu+Cu2++H2O
②几种氢氧化物开始沉淀和完全沉淀的pH如表:
回答下列问题:
(1)固体A 主要由两种物质组成,其化学式为SiO2、Cu.
(2)酸浸、过滤后,滤液中铁元素的存在形式为Fe2+(填离子符号),生成该离子的离子方程式为2Fe3++Cu=2Fe2++Cu2+.
(3)沉淀B的化学式为Fe(OH)3,氧化过程中发生反应的离子方程式为2Fe2++ClO-+2CO32-+3H2O=Fe(OH)3↓+Cl-+2CO2↑.
(4)加NaOH调节溶液pH的范围是5.2≤pH<5.4,工业上对沉淀B、沉淀C的利用应采取的处理方法是加热分解得到相应的氧化物,用于冶炼铁和铝.

已知:①Cu2O+2H+=Cu+Cu2++H2O
②几种氢氧化物开始沉淀和完全沉淀的pH如表:
| 氢氧化物 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 |
| 开始沉淀的pH | 4.0 | 5.8 | 1.1 | 5.4 |
| 完全沉淀的pH | 5.2 | 8.8 | 3.2 | 6.7 |
(1)固体A 主要由两种物质组成,其化学式为SiO2、Cu.
(2)酸浸、过滤后,滤液中铁元素的存在形式为Fe2+(填离子符号),生成该离子的离子方程式为2Fe3++Cu=2Fe2++Cu2+.
(3)沉淀B的化学式为Fe(OH)3,氧化过程中发生反应的离子方程式为2Fe2++ClO-+2CO32-+3H2O=Fe(OH)3↓+Cl-+2CO2↑.
(4)加NaOH调节溶液pH的范围是5.2≤pH<5.4,工业上对沉淀B、沉淀C的利用应采取的处理方法是加热分解得到相应的氧化物,用于冶炼铁和铝.

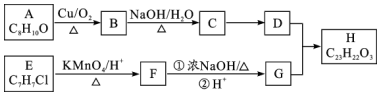
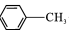 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$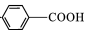
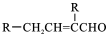
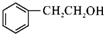 ,C→D的反应类型为加成反应;B中含氧官能团名称为醛基,F中不含氧的官能团的名称为氯原子; H的结构简式为
,C→D的反应类型为加成反应;B中含氧官能团名称为醛基,F中不含氧的官能团的名称为氯原子; H的结构简式为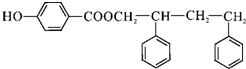 ;
;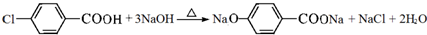 ;
;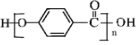 ;
;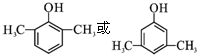 .
.