题目内容
14. 苹果iphone6正在我国热卖,其电池为锂电池.构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
苹果iphone6正在我国热卖,其电池为锂电池.构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )| A. | 该电池放电时的负极材料为LiCoO2 | |
| B. | 电池中的固体电解质可以是熔融的氯化钠、氯化铝等 | |
| C. | 充电时的阴极反应:Li1-xCoO2+xLi++xe-═LiCoO2 | |
| D. | 外电路上的“→”表示放电时的电子流向 |
分析 A、放电时,负极上失电子化合价升高,发生氧化反应;
B、熔融的氯化铝中不含自由移动的离子;
C、充电时,阴极发生还原反应化合降低;
D、放电时,该装置是原电池,原电池工作时,外电路上电流从正极流向负极.
解答 解:A、放电时,负极上失电子化合价升高,发生氧化反应,所以LiCoO2为电池的负极,故A正确;
B、熔融的氯化铝中不含自由移动的离子,不能作电解质,故B错误;
C、充电时,阴极发生还原反应化合降低,所以电极反应式为Li1-xCoO2+xLi++xe-═LiCoO2,故C正确;
D、放电时,电极LiCoO2失电子发生氧化反应作负极,碳棒作正极,外电路上电流从正极沿导线流向负极,所以外电路上的“→”表示放电时的电子方向,故D正确;
故选B.
点评 本题以新型电池为载体考查了原电池和电解池原理,难度较大,能根据电池反应式正确判断原电池和电解池反应是解本题的关键.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
4.为达到预期的实验目的,下列操作中正确的是( )
| A. | 鉴别AlC13溶液和MgC12溶液:向2种待测液中分别滴加足量氨水 | |
| B. | 可用过滤法分离氢氧化铁胶体和三氯化铁溶液的混合物 | |
| C. | 除去Fe(OH)3固体中少量Mg(OH)2:加入足量浓FeCl3溶液,充分搅拌过滤 | |
| D. | 除去铜器表面的铜绿[Cu2(OH)2CO3]:用硝酸浸泡,再用清水冲洗 |
5.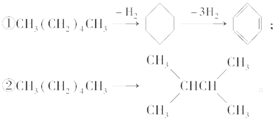 增加汽油中支链烷烃、芳香烃和环烷烃的比例是从根本上提高汽油品质的措施,生产中常用催化重整等方式来实现.例如以下两个在催化重整时发生的反应:则下列叙述不正确的是( )
增加汽油中支链烷烃、芳香烃和环烷烃的比例是从根本上提高汽油品质的措施,生产中常用催化重整等方式来实现.例如以下两个在催化重整时发生的反应:则下列叙述不正确的是( )
 增加汽油中支链烷烃、芳香烃和环烷烃的比例是从根本上提高汽油品质的措施,生产中常用催化重整等方式来实现.例如以下两个在催化重整时发生的反应:则下列叙述不正确的是( )
增加汽油中支链烷烃、芳香烃和环烷烃的比例是从根本上提高汽油品质的措施,生产中常用催化重整等方式来实现.例如以下两个在催化重整时发生的反应:则下列叙述不正确的是( )| A. | 石油分馏后得到的汽油远不能满足需求,故常用裂化等方法生产更多的轻质油 | |
| B. | 使用含铅抗爆剂,会导致铅污染,故目前已禁止使用 | |
| C. | ①②均为消去反应 | |
| D. | ①②反应过程中有机物碳原子数均没有发生变化 |
2.有人设计了以下反应途径制H2,假设反应都能进行,你认为最合理的是( )
| A. | C3H8$\stackrel{极高温}{→}$3C+4H2 | |
| B. | C3H8$\stackrel{高温脱氢}{→}$C3H6+H2 | |
| C. | C3H8+3H2O$\stackrel{催化剂}{→}$3CO+7H2 | |
| D. | C3H8+5O2→3CO2+4H2O,2H2O$\stackrel{电解}{→}$2H2↑+O2↑ |
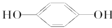 E; ③
E; ③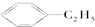 H;
H;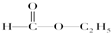 I;⑤
I;⑤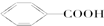 G; ⑥
G; ⑥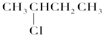 J.
J.
