题目内容
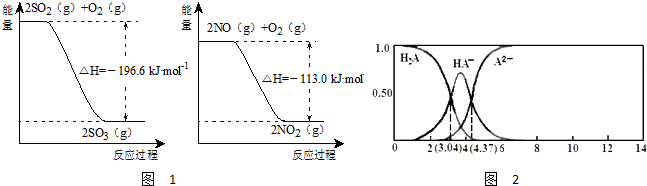
 (1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式(2)W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大.W、Y的氧化物是导致酸雨的主要物质,X是第三周期元素形成的简单阳离子半径最小的元素,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物.
①X的简单阳离子的电子式是
②W的最高价氧化物对应水化物的稀溶液与Z2O反应的化学方程式是
③已知:Fe(s)+
|
2X(s)+
| 3 |
| 2 |
X的单质和FeO反应的热化学方程式是
考点:热化学方程式,用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:(1)通过分析图象,反应物的能量比生成物高,反应放热,反应物的活化能为E1,生成物的活化能为E2,△H=E1-E2,据此分析.
(2)导致酸雨的主要物质是二氧化氮和二氧化硫,且W、X、Y、Z是周期表前36号元素中的四种常见元素,Y的原子序数大于W的,所以W是氮元素,Y是硫元素;X是第三周期元素形成的简单阳离子半径最小的元素,所以X是铝元素;Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物,且Z是前36号元素,Z的原子序数大于Y的,所以Z是铜元素,据此解答.
(2)导致酸雨的主要物质是二氧化氮和二氧化硫,且W、X、Y、Z是周期表前36号元素中的四种常见元素,Y的原子序数大于W的,所以W是氮元素,Y是硫元素;X是第三周期元素形成的简单阳离子半径最小的元素,所以X是铝元素;Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物,且Z是前36号元素,Z的原子序数大于Y的,所以Z是铜元素,据此解答.
解答:
解:(1)反应物的能量比生成物高,反应放热,反应物的活化能为E1,生成物的活化能为E2,故反应的△H=E1-E2,故反应的化学方程式为:NO2(g)+CO(g)═CO2(g)+NO(g),△H=E1-E2=-234KJ/mol.
故答案为:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ?mol-1;
(2)导致酸雨的主要物质是二氧化氮和二氧化硫,且W、X、Y、Z是周期表前36号元素中的四种常见元素,Y的原子序数大于W的,所以W是氮元素,Y是硫元素;X是第三周期元素形成的简单阳离子半径最小的元素,所以X是铝元素;Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物,且Z是前36号元素,Z的原子序数大于Y的,所以Z是铜元素.
①X的简单阳离子即Al3+的电子式即是其离子符号本身,故答案为:Al3+;
②W的最高价氧化物对应水化物的稀溶液即HNO3溶液,与Z2O即Cu2O反应的化学方程式是:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O
故答案为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O;
③已知:Fe(s)+
O2(g)=FeO(s)△H=-272.0kJ?mol-1①
2Al(s)+
O2(g)=Al2O3(s)△H=-1675.7kJ?mol-1②
将方程式②-①×3得:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△HH=-859.7KJ/mol
故答案为:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△H=-859.7KJ/mol.
故答案为:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ?mol-1;
(2)导致酸雨的主要物质是二氧化氮和二氧化硫,且W、X、Y、Z是周期表前36号元素中的四种常见元素,Y的原子序数大于W的,所以W是氮元素,Y是硫元素;X是第三周期元素形成的简单阳离子半径最小的元素,所以X是铝元素;Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物,且Z是前36号元素,Z的原子序数大于Y的,所以Z是铜元素.
①X的简单阳离子即Al3+的电子式即是其离子符号本身,故答案为:Al3+;
②W的最高价氧化物对应水化物的稀溶液即HNO3溶液,与Z2O即Cu2O反应的化学方程式是:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O
故答案为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O;
③已知:Fe(s)+
| 1 |
| 2 |
2Al(s)+
| 3 |
| 2 |
将方程式②-①×3得:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△HH=-859.7KJ/mol
故答案为:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△H=-859.7KJ/mol.
点评:本题考查了元素的推断、核外电子排布、热化学方程式等知识点,难度不答,能正确判断各元素是解本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法正确的是( )
| A、冰熔化时,分子中H-O键发生断裂 |
| B、NaOH中只含有离子键 |
| C、CO2与SiO2都属于分子晶体 |
| D、熔沸点由高到低的顺序是金刚石>NaCl>I2 |
联苯的结构简式如图,下列有关联苯的说法中正确的是( )


| A、分子中含有6个碳碳双键 |
| B、1mol联苯最多可以和6mol H2发生加成反应 |
| C、它容易发生加成反应、取代反应,也容易被强氧化剂氧化 |
D、它和蒽( )同属于芳香烃,两者互为同系物 )同属于芳香烃,两者互为同系物 |

 (1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是(填序号)
(1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是(填序号)