题目内容
1.下列说法中正确的是( )| A. | 胶体区别于其它分散系的本质特性是丁达尔现象 | |
| B. | 利用半透膜可除去淀粉溶液中的少量NaCl | |
| C. | Fe(OH)3胶体带正电荷 | |
| D. | 加入电解质,胶体一定能发生凝聚 |
分析 A.区分分散系的本质特性是分散质粒子的直径大小;
B.胶粒不能透过半透膜;
C.Fe(OH)3胶体不带电荷,是电中性的;
D.有些胶体不带电荷.
解答 解:A.区分分散系的本质特性是分散质粒子的直径大小,胶体微粒直径在1-100nm之间,故A错误;
B.淀粉溶液是胶体,胶粒不能透过半透膜,可用渗析提纯胶体,故B正确;
C.Fe(OH)3胶体不带电荷,是电中性的,胶粒带正电荷,故C错误;
D.有些胶体不带电荷,加入电解质不发生聚沉,故D错误.
故选B.
点评 本题考查了胶体的性质、制取方法等知识,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
11.如图所示的装置,C.D.E.F.X.Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是( )
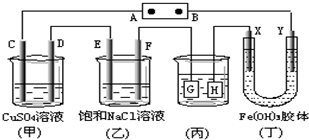

| A. | 电源B极是正极 | |
| B. | 欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 | |
| C. | 甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:2 | |
| D. | 装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带负电荷 |
9.能用H++OH-═H2O表示的化学方程式有( )
| A. | 氢氧化钠溶液与硝酸反应 | B. | 氢氧化铁与硫酸反应 | ||
| C. | 氢氧化钡与硫酸反应 | D. | 硫酸氢钠与氢氧化钠溶液反应 |
16.叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是( )
| A. | HN3水溶液中微粒浓度大小顺序为:c(H+)>c( N3-)>c(HN3)>c(OH-) | |
| B. | NaN3水溶液中离子浓度大小顺序为:c(Na+)>c( N3-)>c(OH-)>c(H+) | |
| C. | HN3与NH3作用生成的叠氮酸铵是强电解质 | |
| D. | N3-与CO2互为等电子体 |
6.某有机物的分子式为C3H6O,通过核磁共振氢谱分析有3个峰,峰面积比例为1:2:3,则该物质可能是( )
| A. | CH3COCH3 | B. | CH3CH2CHO | C. | CH2=CH-CH2OH | D. | CH2=CH-O-CH3 |
13.下列说法正确的是( )
| A. | 凡是放热反应都是自发的,由于吸热反应都是非自发的 | |
| B. | 自发反应一定是熵增大,非自发反应一定是熵减少或不变 | |
| C. | 电解池的反应属于自发过程 | |
| D. | 自发反应在恰当条件下才能实现 |
10.已知一个N2O3分子的质量为a g,一个N2O5分子的质量为b g,若以一个氧原子质量的$\frac{1}{6}$作为相对原子质量的标准,则NO2的相对分子质量为( )
| A. | $\frac{3(a+b)}{b-a}$ | B. | $\frac{16(b+a)}{b-a}$ | C. | $\frac{8(b-a)}{b+a}$ | D. | $\frac{16(b-a)}{b+a}$ |
11.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 18g D2O和18g H2O中含有的质子数均为10NA | |
| B. | PH=1的亚硫酸溶液中含有的H+数目为0.1NA | |
| C. | 2.3 g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1Na | |
| D. | 0.1 mol的Na2O2中含阴离子数是0.2 NA |
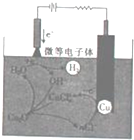 氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂灯领域有着广泛的用途.回答下列问题:
氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂灯领域有着广泛的用途.回答下列问题: