题目内容
10.下列叙述正确的是( )| A. | 乙烯和聚氯乙烯都能使溴的四氯化碳溶液褪色 | |
| B. | 乙烷、丙烷、丁烷都没有同分异构体 | |
| C. | 酒越陈越香与酯化反应有关 | |
| D. | 甲烷与足量氯气在光照下反应可生成难溶于水的油状液体 |
分析 A.聚乙烯不含碳碳双键;
B.丁烷存在正丁烷、异丁烷两种结构;
C.乙醇发生氧化反应生成乙酸,乙醇、乙酸发生酯化反应生成乙酸乙酯;
D.甲烷中H被Cl取代生成氯代烃.
解答 解:A.聚乙烯不含碳碳双键,不能使溴的四氯化碳溶液褪色,乙烯可以,故A错误;
B.丁烷存在正丁烷、异丁烷两种结构,乙烷、丙烷都没有同分异构体,故B错误;
C.乙醇发生氧化反应生成乙酸,乙醇、乙酸发生酯化反应生成乙酸乙酯,则酒越陈越香与酯化反应有关,故C正确;
D.甲烷中H被Cl取代生成氯代烃,则甲烷与足量氯气在光照下反应可生成难溶于水的油状液体,故D正确;
故选CD.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系,下列有关说法正确的是( )

| A. | a点对应的溶液中水的电离程度可能大于c点对应的溶液中水的电离程度 | |
| B. | 将25℃时的NaCl溶液加热到T℃,则该溶液中的c(OH-)由b点变化到e点 | |
| C. | bd线上的任意一点均有pH=7 | |
| D. | a点对应的溶液中大量存在的离子可能为:NH4+、Ba2+、NO3-、F- |
1.化学与生活、社会密切相关,下列说法不正确的是( )
| A. | “地沟油”禁止食用,但经加工处理后可用来制造肥皂和生物柴油 | |
| B. | 白铁(镀锌铁板)比马口铁(镀锡铁板)更耐腐蚀 | |
| C. | 牺牲阳极的阴极保护法是应用电解原理防止金属的腐蚀 | |
| D. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+2×283.0KJ/mol |
18.下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.086 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | L、R形成的简单离子核外电子数相等 | |
| B. | 单质与浓度相等的稀盐酸反应的速率为Q>L | |
| C. | 氢化物的稳定性为H2T<H2R | |
| D. | M与T形成的化合物既能与强酸反应又能与强碱反应 |
5.下列关于有机物的说法正确的是( )
| A. | 天然气为纯净物 | |
| B. | 天然气是不可再生的能源 | |
| C. | 乙烯的结构简式为CH2CH2 | |
| D. | 过量的CH4和Cl2在光照条件下反应只生成CH3Cl |
15.NaH可用作生氢剂,反应的化学方程式是NaH+H2O═NaOH+H2↑.则下列说法正确的是( )
| A. | NaOH是氧化产物 | B. | 该反应电子转移数为2e- | ||
| C. | NaH为还原剂 | D. | H2O既是还原剂又是氧化剂 |
19. 某同学按如图所示的装置做实验,并记录实验情况.你认为框内叙述合理的是( )
某同学按如图所示的装置做实验,并记录实验情况.你认为框内叙述合理的是( )
①锌为正极,铜为负极?
②电解质溶液的pH不变?
③电流表的指针发生偏转?
④铜极上有气泡产生?
⑤锌极上仍有少量气泡产生?
⑥溶液中的阳离子向负极移动.
 某同学按如图所示的装置做实验,并记录实验情况.你认为框内叙述合理的是( )
某同学按如图所示的装置做实验,并记录实验情况.你认为框内叙述合理的是( ) ①锌为正极,铜为负极?
②电解质溶液的pH不变?
③电流表的指针发生偏转?
④铜极上有气泡产生?
⑤锌极上仍有少量气泡产生?
⑥溶液中的阳离子向负极移动.
| A. | ①②③ | B. | ③④⑤ | C. | ③④⑥ | D. | ②③④ |
20.下列三种有机物是某些药物中的有效成分:

以下说法正确的是( )

以下说法正确的是( )
| A. | 将各1mol的三种物质分别与氢氧化钠溶液充分反应,阿司匹林消耗氢氧化钠最多 | |
| B. | 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 | |
| C. | 三种有机物中的所有原子不可能共平面 | |
| D. | 三种有机物都能与浓溴水发生反应 |
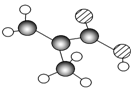 某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).
某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键). .
. .
.