题目内容
我国拥有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务.海水的综合利用可以得到金属镁等产品,其流程如图所示:

(1)向母液中加入石灰乳制得Mg(OH)2,写出该反应的离子方程式: .
(2)电解熔融的MgCl2可以得到金属镁时,写出相应的反应的化学方程式: .
(3)实验室里将粗盐制成精盐的过程中,溶解、过滤、蒸发三个步骤的操作都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的作用:
溶解时: ;
过滤时: ;
蒸发时: .

(1)向母液中加入石灰乳制得Mg(OH)2,写出该反应的离子方程式:
(2)电解熔融的MgCl2可以得到金属镁时,写出相应的反应的化学方程式:
(3)实验室里将粗盐制成精盐的过程中,溶解、过滤、蒸发三个步骤的操作都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的作用:
溶解时:
过滤时:
蒸发时:
考点:海水资源及其综合利用
专题:实验设计题
分析:(1)海水中含有镁离子,加入石灰乳生成氢氧化镁;
(2)电解熔融的MgCl2可以得到金属镁和氯气;
(3)根据粗盐提纯实验操作判断玻璃棒的作用.
(2)电解熔融的MgCl2可以得到金属镁和氯气;
(3)根据粗盐提纯实验操作判断玻璃棒的作用.
解答:
解:(1)海水中含有镁离子,加入石灰乳生成氢氧化镁,发生反应离子方程式为:Mg2++2OH-=Mg(OH)2,故答案为:Mg2++2OH-=Mg(OH)2;
(2)电解熔融的MgCl2可以得到金属镁和氯气,反应化学方程式为MgCl2
Mg+Cl2↑,故答案为:MgCl2
Mg+Cl2↑;
(3)在溶解时,使用玻璃棒搅拌,加速溶解;过滤时,使用玻璃棒引流,防止液体流出;蒸发时,使用玻璃棒搅拌,使液体受热均匀,防止溅出,
故答案为:搅拌;引流;搅拌.
(2)电解熔融的MgCl2可以得到金属镁和氯气,反应化学方程式为MgCl2
| ||
| ||
(3)在溶解时,使用玻璃棒搅拌,加速溶解;过滤时,使用玻璃棒引流,防止液体流出;蒸发时,使用玻璃棒搅拌,使液体受热均匀,防止溅出,
故答案为:搅拌;引流;搅拌.
点评:本题考查了离子方程式和电解方程式的书写,以及粗盐提纯中玻璃棒的作用,难度不大,属于基础性知识的考查.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
化学工作者从有机反应RH+Cl2(g)═RCl(l)+HCl(g)中受到启发,提出的在农药和有机合成工业中可获得副产品盐酸的设想已成为现实.试指出从上述反应产物中分离得到盐酸的最佳方法是(g表示物质为气态,l表示物质为液态.HCl极易溶于水,得到盐酸;有机物一般难溶于水)( )
| A、蒸馏法 | B、水洗分液法 |
| C、升华法 | D、有机溶剂萃取法 |
关于如图装置说法正确的是( )


| A、装置中电子移动的途径是:负极→Fe→M溶液→石墨→正极 |
| B、若M为FeCl2溶液,可以实现石墨上镀铁 |
| C、若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
| D、若 M为NaCl溶液,通电段时间后,溶液中可能有NaClO |
下列现象不属于蛋白质变性的是( )
| A、蛋白溶液中加入食盐变浑浊 |
| B、用稀的福尔马林浸泡种子 |
| C、打针时用酒精消毒 |
| D、用波尔多液(由CuSO4溶液、生石灰和水制成)防止作物虫害 |
硬铝是制造飞机和宇宙飞船的理想材料,下列哪一项不应该是硬铝的性能( )
| A、加工性差 | B、强度高 |
| C、抗腐蚀 | D、密度小 |
用NA表示阿伏加德罗常数的值.下列说法正确是( )
| A、标准状况下,2.24 L二氧化碳中含有共用电子对的数目为0.2NA |
| B、25℃时,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA |
| C、0.1mol Cl2与足量铁粉反应转移电子的数目为0.2NA |
| D、标准状况下,2.24L O2和1.12L NO混合后的气体分子总数为0.15×6.02×1023 |
 在某有机物A的分子中,具有醇羟基、羧基等官能团,其结构简式如图.
在某有机物A的分子中,具有醇羟基、羧基等官能团,其结构简式如图.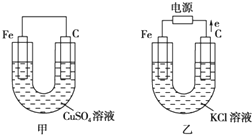 根据如图所提供的信息,在反应一段时间后:
根据如图所提供的信息,在反应一段时间后: