题目内容
12.下列各物质中所含分子个数由大小的顺序正确的是( )①0.6molNH3;②标准状况下22.4L氦气;③4℃时9mL水;④0.2molH3PO4.
| A. | ①④③② | B. | ④③②① | C. | ②①③④ | D. | ①④②③ |
分析 根据n=$\frac{V}{{V}_{m}}$氦气物质的量,故m=ρV计算水的质量,再根据n=$\frac{m}{M}$计算水的物质的量,物质的量越大含有的分子数目越多.
解答 解:①0.6molNH3;②标准状况下22.4L氦气的物质的量$\frac{22.4L}{22.4L/mol}$=1mol;③4℃时9mL水的质量为9g,其物质的量为$\frac{9g}{18g/mol}$=0.5mol;④0.2molH3PO4,由N=nNA可知,物质的量越大含有的分子数目越多,故含有分子数目:②>①>③>④,
故选C.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的有关计算.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
2.下列叙述正确的是( )
| A. | 金属镁工业冶炼的方法是采用直接加热分解法 | |
| B. | 石油是由多种碳氢化合物组成的混合物 | |
| C. | 煤的主要成分是碳单质 | |
| D. | 酸雨的形成主要是由于CO2含量过高 |
3.在溶液中含有的物质至少有( )
| A. | 一种 | B. | 两种 | C. | 三种 | D. | 四种 |
17.四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
请回答下列问题:
(1)元素Z位于周期表中的位置第三周期VA族;
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(写化学式);
(3)XW2的电子式为 ;
;
(4)Y的最高价氧化物的化学式为N2O5;
(5)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%.该化合物的化学式为S4N4.
| X | Y | |
| Z | W |
(1)元素Z位于周期表中的位置第三周期VA族;
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(写化学式);
(3)XW2的电子式为
 ;
;(4)Y的最高价氧化物的化学式为N2O5;
(5)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%.该化合物的化学式为S4N4.
4.下列不能用勒夏特列原理解释的是( )
| A. | 棕红色NO2加压后颜色先变深后变浅 | |
| B. | Fe(SCN)3溶液中加入固体KSCN后颜色变深 | |
| C. | 氯水宜保存在低温、避光条件下 | |
| D. | SO2催化氧化成SO3的反应,往往加入过量的空气 | |
| E. | 打开易拉罐有大量气泡冒出 | |
| F. | 加催化剂,使氮气和氢气在一定条件下转化为氨气 |
2.天然气的主要成分是CH4.在一定条件下,可与天然气发生化学反应的是( )
| A. | 氧气(光照) | B. | 氯气(加热) | ||
| C. | 高锰酸钾酸性溶液 | D. | 浓硫酸 |
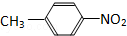 和
和