题目内容
【题目】现用物质的量的浓度为a mol/L的标准盐酸去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是 .
(2)如图是酸式滴定管中液面在滴定前后的读数:则c (NaOH)=moL/L. 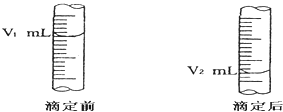
(3)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度会偏 .
【答案】
(1)用标准盐酸润洗2﹣3次
(2)![]()
(3)高
【解析】解:(1)滴定管使用前应用待测液润洗,所以答案是:用标准盐酸润洗2﹣3次;(2)中和滴定中盐酸和NaOH的物质的量相等,(V2﹣V1)a=c (NaOH)V,所以答案是: ![]() ;(3)滴定前酸式滴定管尖嘴部分有气泡,滴定后尖嘴部分充满溶液,会导致体积读数偏大,测量结果偏大,
;(3)滴定前酸式滴定管尖嘴部分有气泡,滴定后尖嘴部分充满溶液,会导致体积读数偏大,测量结果偏大,
所以答案是:偏高.
【考点精析】认真审题,首先需要了解酸碱中和滴定(中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点).

练习册系列答案
相关题目
【题目】工业上常用高炉来进行炼铁,其原理如下。
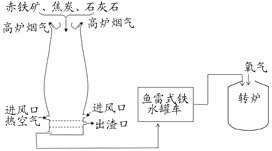
(1)用CO和赤铁矿(Fe2O3)炼铁的化学反应方程式是_________。
(2)请从A或B两题中任选一个作答,若两题都作答,按A计分。
A | B |
用含氧化铁160t的赤铁矿炼铁,理论上可以制得纯铁_____t 。 | 工业上也常用主要成分为四氧化三铁的磁铁矿做炼铁原料。四氧化三铁中铁元素的质量分数计算式为______×100%。 |



