��Ŀ����
��16�֣�
��֪CH3COOH��������Ϊ60��CH3COOCH3��������Ϊ74��
����ֻ��C��H��O�Ļ�����A��F(��ͬ�Ĺ����������ڲ�̼ͬԭ���ϣ�A��һ±����
ֻ��һ��)���й����ǵ�ijЩ��Ϣ����ע��������ķ����ڣ�
��1���ڻ�����A��F�У������Ľṹ�Ļ������ǣ���д��ĸ���ţ��� ��
��2��A��C�Ľṹ��ʽ��
A ��C ��
��3��д��A�����Ƶ�������ͭ��Һ���ȵĻ�ѧ����ʽ�� ��
��4��д��F�����������������Һ���ȵĻ�ѧ����ʽ�� ��
��5��G��B��ͬ���칹�壬��G������������������
�� G�Ƿ����廯����ֻ��һ�ֹ����š�
��1molGǡ������3mol����������Һ��Ӧ
��G�����в���������ͬһ�ֹ����Ų�������һ��̼ԭ���ϡ�
������������ͬ���칹���У� �֡�����д���֣�
��
��1��BCEF
(2) ��
��3��+6Cu(OH)2
+3Cu2O��+6H2O.
��4����4NaOH
CH3COONa��3CH3OH��
��5��6 ��
��
����:A��������������B��A�к����ǻ���B�ķ�������186��B�е�ȩ�������������Ȼ�����Ϊ1��ȩ�������Ȼ�������������16��C��B���48������B�к���3��ȩ������A��Ҳ����3��ȩ����A����ͬ�Ĺ����������ڲ�̼ͬԭ���ϣ���A��һ±����ֻ��һ��
���Ը���A�ķ������ɵó���ṹ��ʽΪ����B��C��D��E��F�ֱ�Ϊ
��
��
��
��
��1molGǡ������3mol����������Һ��Ӧ��˵�������Ȼ�����ǻ���G�Ƿ����廯����ֻ��һ�ֹ����ţ���˹��������ǻ�������ΪG�����в���������ͬһ�ֹ����Ų�������һ��̼ԭ���ϣ����Ա��������ӵ�ȡ������3�����ǻ���1����CHOHCH2OH����˹���6�֡�����
��
�ȡ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| ij�¶��£���֪CH3COOH��HClO��H2CO3��H3PO4 ����ƽ�ⳣ�����±���ʾ����0.1mol?L-1�����и���ҺpH�����ǣ������� ������������ĵ���ƽ�ⳣ��
|
 ��ҵ�ϳ����ô�����Ҵ��ϳ��л��ܼ�����������CH3COOH��l��+C2H5OH��l��
��ҵ�ϳ����ô�����Ҵ��ϳ��л��ܼ�����������CH3COOH��l��+C2H5OH��l��| ŨH2SO4 |
| �� |
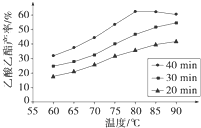
��֪CH3COOH��C2H5OH��CH3COOC2H5�ķе�����Ϊ118�桢78���77�森������������ͬʱ��ij�о�С������˶��ʵ�飬ʵ������ͼ��ʾ����1�����о�С���ʵ��Ŀ����
��2��60���·�Ӧ40min��70���·�Ӧ20min��ȣ�ǰ�ߵ�ƽ����Ӧ����
��3����ͼ��ʾ����Ӧʱ��Ϊ40min���¶ȳ���80��ʱ���������������½���ԭ�������
��ú�����г����о���ͬ�¶���ƽ�ⳣ����Ͷ�ϱȼ���ֵ�����⣮
��֪��CO��g��+H2O��g��??H2��g��+CO2��g��ƽ�ⳣ�����¶ȵı仯���±���
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
��1����800�淢��������Ӧ���Ա��е����ʵ���Ͷ����ݷ�Ӧ��������������Ӧ�����ƶ�����
| n��CO�� | n��H2O�� | n��H2�� | n��CO2�� | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
C��s��+H2O��g��??CO��g��+H2��g����ƽ�ⳣ��ΪK1��
CO��g��+H2O��g��??H2��g��+CO2��g����ƽ�ⳣ��ΪK2��
��K��K1��K2֮��Ĺ�ϵ��
��3����V L�ܱ�������ͨ��10mol CO��10molˮ��������T��ﵽƽ�⣬Ȼ����ͨ����ʯ�ң������û������ȼ�գ���÷ų�������Ϊ2 842kJ����֪COȼ����Ϊ283kJ?mol-1��H2ȼ����Ϊ286kJ?mol-1������T��ƽ�ⳣ��K=