题目内容
4. 钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛应用.
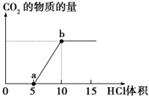
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛应用.(1)如图表示的是向Na2CO3溶液中滴入稀盐酸时产生CO2的过程.
写出0到a点发生反应的离子方程式:CO32-+H+=HCO3-.
(2)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,可应用于汽车安全气囊.请写出其反应的化学方程式2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑.
(3)现有一Na2CO3和NaHCO3的混合物样品,取ag该混合物充分加热,减重bg则该混合物样品中Na2CO3的质量分数是$\frac{31a-84b}{31a}$;
(4)钠一钾合金可在核反应堆中用作热交换液.5.05g钠一钾合金溶于200mL水生成0.075mol氢气.则该溶液中氢氧根离子的物质的量浓度是0.75(mol/L);(忽略溶液体积变化).
分析 (1)碳酸钠和少量的盐酸之间反应生成的是碳酸氢钠和氯化钠;
(2)根据反应物和生成物及其质量守恒定律书写化学方程式;
(3)NaHCO3不稳定,加热易分解,根据质量的变化利用差值法解答;
(4)结合反应的方程式2Na+2H2O═2NaOH+H2↑、2K+2H2O═2KOH+H2↑计算.
解答 解:(1)碳酸钠和少量的盐酸之间反应生成的是碳酸氢钠和氯化钠,离子方程式为CO32-+H+=HCO3-,故答案为:CO32-+H+=HCO3-;
(2)叠氮化钠分解生成钠和氮气,反应的化学方程式为:2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑;
故答案为:2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑;
(3)NaHCO3不稳定,加热易分解,发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
则2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑△m
168g 106g 62g
x bg
x=$\frac{168b}{62}$g,
则样品中Na2CO3的质量为ag-$\frac{168b}{62}$g=$\frac{62a-168b}{62}$g,
所以该混合物样品中Na2CO3的质量分数是$\frac{62a-168b}{62a}$=$\frac{31a-84b}{31a}$,
故答案为:$\frac{31a-84b}{31a}$;
(4)设钠、钾的物质的量分别为a、b,反应的方程式为2Na+2H2O═2NaOH+H2↑、2K+2H2O═2KOH+H2↑,
则a+b=0.075mol×2=0.15mol,
该溶液中氢氧根离子的物质的量浓度是$\frac{0.15mol}{0.2L}$=0.75mol/L,
故答案为:0.75(mol/L).
点评 本题考查较为综合,涉及碱金属的单质以及混合物的性质,侧重于学生的分析能力和计算能力的考查,注意把握题给信息,学习中注意相关基础知识的积累,根据反应的方程式解答该题,难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 明矾-净化水 | B. | 漂白粉-漂白织物 | C. | 食醋-除水垢 | D. | 纯碱-去油污 |
| A. | 选用480 mL容量瓶,称取12.0g硫酸铜,配成480mL溶液 | |
| B. | 选用250 mL容量瓶,称取12.5g胆矾,配成500mL溶液 | |
| C. | 选用500 mL容量瓶,称取12.5g胆矾,加入500mL水 | |
| D. | 选用500 mL容量瓶,称取12.5g胆矾,配成500mL溶液 |
| A. | Na2O2是淡黄色固体,Na2O 是白色固体,二者都能与水反应生成 NaOH | |
| B. | Na和O2在加热时反应生成 Na2O2,在常温下反应生成 Na2O | |
| C. | Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成 O2 | |
| D. | 2 g H2充分燃烧后产物被Na2O2完全吸收,Na2O2固体增重2g |
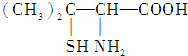
(分子中的-SH与-OH具有类似性质).下列关于青霉氨基酸的推断合理的是( )
| A. | 青霉氨基酸分子中所有碳原子均在同一直线上 | |
| B. | 青霉氨基酸具有两性并能发生酯化反应 | |
| C. | 青霉氨基酸分子间不能发生缩合反应 | |
| D. | 1 mol青霉氨基酸与足量的金属钠反应生成0.5 mol H2 |
 .P元素属于p区元素,
.P元素属于p区元素,

 (用元素符号表示)
(用元素符号表示)
