题目内容
酸雨既可导致土壤酸化影响植物正常生长发育,还能损坏建筑设施.下列各选项中的两种物质都能导致酸雨形成的是( )
| A、二氧化氮和二氧化碳 | B、一氧化碳和二氧化碳 | C、二氧化硫和二氧化碳 | D、二氧化硫和二氧化氮 |
考点:二氧化硫的污染及治理
专题:元素及其化合物
分析:正常的雨水由于溶解了二氧化碳,pH值为5.6,酸雨是指PH小于5.6的雨雪或其他形式的降水,.雨、雪等在形成和降落过程中,吸收并溶解了空气中的二氧化硫、氮氧化合物等物质,形成了pH低于5.6的酸性降水.
解答:解:正常的雨水由于溶解了二氧化碳,pH值为5.6,酸雨是指PH小于5.6的雨雪或其他形式的降水,.雨、雪等在形成和降落过程中,吸收并溶解了空气中的二氧化硫、氮氧化合物等物质,形成了pH低于5.6的酸性降水.
硫酸型酸雨:SO2+H2O=H2SO3、2H2SO3+O2→2H2SO4
硝酸型酸雨:3NO2+H2O=2HNO3+NO,
故选D.
硫酸型酸雨:SO2+H2O=H2SO3、2H2SO3+O2→2H2SO4
硝酸型酸雨:3NO2+H2O=2HNO3+NO,
故选D.
点评:本题考查了酸雨的形成,难度不大,注意各种环境污染的成因和治理方法,如酸雨、光化学烟雾、赤潮、臭氧空洞等,保护环境,人人有责.

练习册系列答案
相关题目
下列各物质所含原子数目,按由大到小顺序排列的是
①0.5mol NH3 ②标准状况下22.4 L He ③4℃ 9mL 水 ④0.2mol H3PO4
A.④③②① B.①④③②
C.①④②③ D.②③④①
(12分)已知反应2HI(g)  H2(g) +I2(g)在T℃下的平衡常数为0.01。T℃时,在容积为2L的密闭容器中加入HI ,反应到某时刻测得各组分的浓度如下:
H2(g) +I2(g)在T℃下的平衡常数为0.01。T℃时,在容积为2L的密闭容器中加入HI ,反应到某时刻测得各组分的浓度如下:
物质 | HI | H2 | I2 |
浓度/(mol·L-1) | 0.40 | 0.60 | 0.60 |
请计算回答下列问题(写出计算过程,否则不得分):
(1)起始加入HI的物质的量 mol。
(2)达到平衡后HI的物质的量浓度 mol·L-1(请保留三位有效数字)。
(3)T℃时,在另一个体积一定的密闭容器中,将I2(g)与H2(g) 置于其中发生上述反应,若达到平衡时H2(g)与I2(g)的体积比为1∶4,计算平衡时HI的体积分数为 ,以及开始时H2(g)与I2(g)的体积比为 。
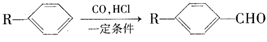
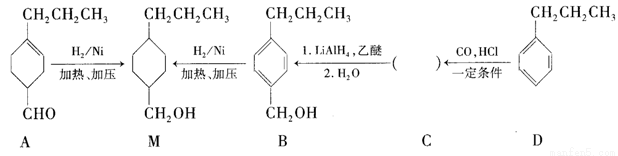
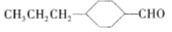 和______(写结构简式)生成。
和______(写结构简式)生成。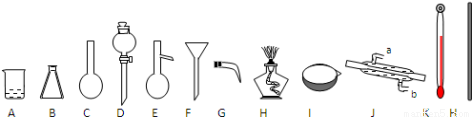
 CO(g) ΔH=-110.5 kJ·mol-1②Mg(g)+O2(g)
CO(g) ΔH=-110.5 kJ·mol-1②Mg(g)+O2(g) Mg(g)+CO(g),该反应的ΔH= 。
Mg(g)+CO(g),该反应的ΔH= 。