题目内容
【题目】不同条件下,用O2氧化a mol/L FeCl2溶液过程中所 测的实验数据如图所示。下列分析或推测合理的是
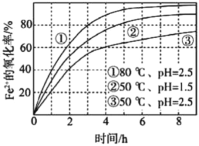
A.由①、②可知,pH越大,+2价铁越易被氧化
B.由②、③推测,若pH>7,+2价铁更难被还原
C.由①、③推测,FeCl2被O2氧化的反应为放热反应
D.60℃、pH=2.5时,4 h内Fe2+的平均消耗速率大于0.15a mol/(L·h)
【答案】D
【解析】
A.①、②中温度和pH均不同,存在两个变量,不能判断pH对反应的影响,故A错误;
B.若pH>7,+2价铁会转化为氢氧化亚铁沉淀,氢氧化亚铁在空气中能被氧气氧化生成氢氧化铁,所以+2价铁易被氧化,故B错误;
C.①、③中pH相同,温度越高,转化率越大,则FeCl2被O2氧化的反应为吸热反应,故C错误;
D.50℃、pH=2.5时,4h内Fe2+的平均消耗速率等于0.15amol/(Lh),在60℃、pH=2.5时,温度升高,速率增大,所以60℃、pH=2.5时,4h内Fe2+的平均消耗速率大于0.15amol/(Lh),故D正确。
故答案为D。

【题目】实验室用卤块(主要成分为MgCl2·6H2O,含有MgSO4.FeCl2等杂质)制备少量Mg(ClO3)2·6H2O的流程如下:
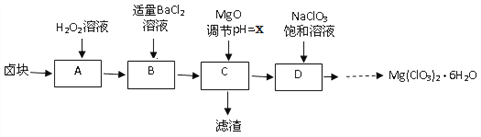

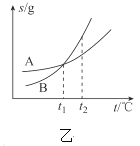
已知:①四种化合物的溶解度(S)随温度(T)变化曲线如图所示。
②室温时一些物质的Ksp如下表:
化学式 | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 |
Ksp | 8.0×10-16 | 8.0×10-38 | 1.8x10-11 |
③Mg(ClO3)2有较强的氧化性,其还原产物是Cl-.
(1)H2O2的电子式为_________
(2)滤渣的成分是____________(填化学式);
(3)经测定,D中铁离子的浓度为1×10-5 mol/L,则x为______
(4)D中所发生的化学反应方程式为_____,框图中由D→......→制Mg(ClO3)2·6H2O晶体的实验步骤依次为:①加热蒸发;②_______(请补充);③冷却结晶;④过滤洗涤。
(5)产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10.00 mL试液于锥形瓶中,加入10.00 mL稀硫酸和20 .00mL 1.000 mol/L的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7溶液滴定剩余的Fe2+至终点。
步骤4:将步骤2、3重复两次
①步骤3中发生反应的离子方程式____________
②步骤3中若滴定前不用标准液润洗滴定管,将会导致最终结果_____(填“偏大”. “偏小”或“不变”)。
③若平均消耗K2Cr2O7溶液15.00 mL,则产品中Mg(ClO3)2·6H2O(其M=299g/mol)的质量分数为___________
【题目】下表中列出了25C、101kPa时一些物质的燃烧热数据
物质 | CH4 | C2H2 | H2 |
燃烧热/( kJ·mol-1) | 890.3 | 1299.6 | 285.8 |
已知键能:C—H键:413.4 kJ·mol-1、H—H键:436 kJ·mol-1,乙炔的结构是为H—C![]() C—H则下列叙述正确的是( )
C—H则下列叙述正确的是( )
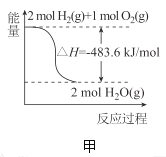
A.2H2(g) + 2O2(g) = 2H2O(g) ΔH = -571.6 kJ·mol-1
B.CH4和C2H2中所含化学键完全相同
C.2CH4(g) = C2H2(g) + 3H2(g) ΔH = -376.4 kJ·mol-1
D.C![]() C键能为796 kJ·mol-1
C键能为796 kJ·mol-1