题目内容
只含碳、氢、氧三种元素的有机物完全燃烧时,消耗的氧气和生成的二氧化碳的体积比是1:2,这类有机物中( )
| A、相对分子质量最小的化合物的化学式为CH2O | B、相对分子质量最小为46 | C、含相同氢原子数的此类化合物,其相对分子质量之差是28的整数倍 | D、含相同碳原子数的此类化合物,其相对分子质量之差是16的整数倍 |
分析:根据只含只含碳、氢、氧三种元素的有机物完全燃烧时,消耗的氧气和生成的二氧化碳的体积比是1:2,则该有机物分子组成可表示为(CO)m(H2O)n,据此分析判断.
解答:解:只含碳、氢、氧三种元素的有机物完全燃烧时,消耗的氧气和生成的二氧化碳的体积比是1:2,则该有机物分子组成可表示为(CO)m(H2O)n.
A、由于该有机物分子组成表示为(CO)m(H2O)n,当m=n=1时,相对分子质量最小,该有机物分子式为CH2O2,故A错误;
B、由于该有机物分子组成表示为(CO)m(H2O)n,当m=n=1时,相对分子质量最小,为46,故B正确;
C、由于该有机物分子组成表示为(CO)m(H2O)n,含相同碳原子的化合物,其相对分子质量差是18的倍数,故C错误;
D、由于该有机物分子组成表示为(CO)m(H2O)n,含相同碳原子的化合物,其相对分子质量差是18的倍数,故D错误.
故选B.
A、由于该有机物分子组成表示为(CO)m(H2O)n,当m=n=1时,相对分子质量最小,该有机物分子式为CH2O2,故A错误;
B、由于该有机物分子组成表示为(CO)m(H2O)n,当m=n=1时,相对分子质量最小,为46,故B正确;
C、由于该有机物分子组成表示为(CO)m(H2O)n,含相同碳原子的化合物,其相对分子质量差是18的倍数,故C错误;
D、由于该有机物分子组成表示为(CO)m(H2O)n,含相同碳原子的化合物,其相对分子质量差是18的倍数,故D错误.
故选B.
点评:本题主要考查有机物燃烧耗氧量与生成二氧化碳的量的关系,难度中等,关键根据消耗的氧气和生成的二氧化碳的体积比是1:2,确定机物分子组成可表示为(CO)m(H2O)n.

练习册系列答案
相关题目



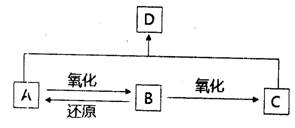
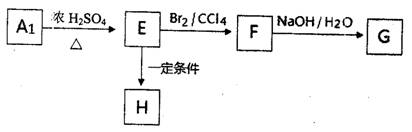
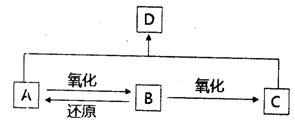
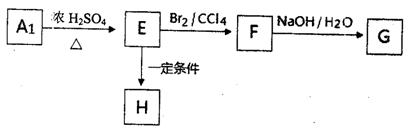
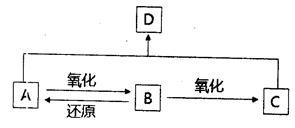
 B分子中含氧官能团的名称是 。
B分子中含氧官能团的名称是 。 。
。