题目内容
【题目】氢气用于烟气的脱氮、脱硫的反应:4H2(g)+2NO(g)+SO2(g)![]() N2(g)+S(l)+4H2O(g)ΔH<0。下列有关说法正确的是( )
N2(g)+S(l)+4H2O(g)ΔH<0。下列有关说法正确的是( )
A.当v(H2)=v(H2O)时,达到平衡
B.升高温度,正反应速率减小,逆反应速率增大,化学平衡逆向移动
C.使用高效催化剂可提高NO的平衡转化率
D.化学平衡常数表达式为K=![]()
【答案】D
【解析】
A. 达到平衡状态时,正反应速率等于逆反应速率;
B. 升高温度,正逆反应速率均增大;
C. 加入催化剂,反应速率加快,平衡不移动;
D. 平衡常数是生成物浓度的幂之积与反应物浓度的幂之积的比值。
A. 没有说明反应速率的方向,不能证明v(正)=v(逆),因此不能判断是否达到平衡,A项错误;
B. 升高温度,正、逆反应速率都增大,B项错误;
C. 加入催化剂,反应速率加快,平衡不移动平衡转化率不变,C项错误;
D. 化学平衡常数为达到平衡时生成物浓度的幂之积与反应物浓度的幂之积的比值,K=![]() ,D项正确;
,D项正确;
答案选D。

 名校课堂系列答案
名校课堂系列答案【题目】I.根据表格信息,请回答下列问题:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
(1)反应①是________(填“吸热”或“放热”)反应。
(2)写出反应③的平衡常数K3的表达式_______________________。
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=________(用K1、K2表示)。
(4)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有____(填写字母序号)。
A.缩小反应容器的容积B.扩大反应容器的容积
C.升高温度D.使用合适的催化剂
E.设法减小平衡体系中的CO浓度
(5)若反应③的逆反应速率与时间的关系如图所示:
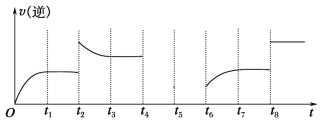
①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时________;t8时________。
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线。__________
Ⅱ.25℃,1.01×105Pa时,16g液态甲醇(CH3OH)完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式__________