题目内容
10.草酸(HOOC-COOH,可简写为H2C2O4),为弱电解质,属于二元中强酸,易溶于水,可用于除锈,织物漂白等.Ⅰ.探究草酸的部分化学性质,进行如下实验.
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量草酸溶液,观察到有无色气泡产生,请写出该反应的离子方程式:HCO3-+H2C2O4=HC2O4-+CO2↑+H2O
(2)向盛有草酸饱和溶液的试管中滴入几滴酸性KMnO4溶液,振荡,溶液的紫红色褪去,说明草酸具有还原性(选填“氧化性”“还原性”或“酸性”),请配平该反应的离子方程式:
2MnO${\;}_{4}^{-}$+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
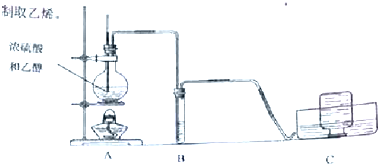
Ⅱ.工业上制备草酸的简要流程如下:

请完成下列填空
(3)已知步骤Ⅰ生成甲酸钠,步骤Ⅱ加热放出H2,请写出操作Ⅱ的化学反应方程式:2HCOONa$\stackrel{△}{→}$Na2C2O4+H2↑
(4)步骤Ⅲ和Ⅳ都是过滤,滤渣分别为CaC2O4和CaSO4,则试剂a和试剂b的化学式分别为Ca(OH)2 H2SO4
(5)将草酸溶液经蒸发浓缩,冷却结晶,过滤洗涤干燥等操作,最终获得草酸晶体.
分析 (1)草酸的酸性比碳酸强,故草酸与碳酸氢钠反应生成二氧化碳,由于草酸足量,故生成NaHC2O4,若写成Na2C2O4是错误的;
(2)酸性高锰酸钾具有强氧化性,草酸具有还原性,能被酸性高锰酸钾氧化;根据得失电子守恒和电荷守恒配平离子方程式;
(3)加热条件下,甲酸钠脱氢生成Na2C2O4和H2;
(4)根据题意Na2C2O4与Ca(OH)2 反应得到CaC2O4和NaOH,过滤得滤渣CaC2O4,加入H2SO4,H2SO4与CaC2O4反应生成CaSO4和H2C2O4,过滤得滤渣CaSO4;
(5)从溶液中制取晶体,一般采用蒸发结晶、过滤、洗涤、干燥的方法.
解答 解:(1)草酸的酸性比碳酸强,故草酸与碳酸氢钠反应生成二氧化碳,由于草酸足量,故还生成NaHC2O4,反应离子方程式为:HCO3-+H2C2O4=HC2O4-+CO2↑+H2O;
故答案为:HCO3-+H2C2O4=HC2O4-+CO2↑+H2O;
(2)酸性KMnO4溶液具有强氧化性,向盛有草酸饱和溶液的试管中滴入几滴酸性KMnO4溶液,振荡,溶液的紫红色褪去,说明草酸被酸性高锰酸钾氧化,具有还原性;
根据氧化还原反应方程式的配平原则:得失电子守恒、质量守恒和电荷守恒配平该反应的离子方程式:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
故答案为:还原性;2 5 6 2 10 8;
(3)加热条件下,甲酸钠脱氢生成Na2C2O4和H2,方程式为:2HCOONa$\stackrel{△}{→}$Na2C2O4+H2↑;
故答案为:2HCOONa$\stackrel{△}{→}$Na2C2O4+H2↑;
(4)Na2C2O4与Ca(OH)2 反应得到CaC2O4和NaOH,过滤得滤渣CaC2O4,加入H2SO4,H2SO4与CaC2O4反应生成CaSO4和H2C2O4,过滤得滤渣CaSO4,滤液H2C2O4溶液;
故答案为:Ca(OH)2;H2SO4;
(5)从溶液得到草酸晶体,需要经蒸发浓缩、冷却结晶、过滤洗涤、干燥,
故答案为:过滤洗涤.
点评 主要考查了草酸的性质与制备,涉及知识点较多,综合性较强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力.

| A. | 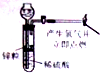 制备并检验氢气的可燃性 | B. | 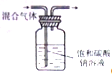 除去CO2中的HCl | ||
| C. | 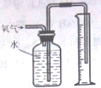 测量O2的体积 | D. | 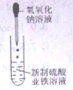 制备氢氧化亚铁并观察其颜色 |
 (1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/molN2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol
若有17g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为226.3kJ.
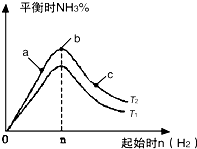
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)?2NH3(g)反应的影响.实验结果如图所示:
(图中T表示温度,n表示物质的量)
①图象中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)═4NO2(g)+O2(g)△H>0下表为反应在T1温度下的部分实验数据
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
| A. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2 | |
| B. | 氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ | |
| D. | 钢铁发生电化学腐蚀的负极反应式:Fe-3e-═Fe3+ |
| A. | 一个自发反应,反应物的总能量必须高于生成物的总能量 | |
| B. | 在等温条件下,化学反应的热效应称为焓变 | |
| C. | 化学反应中,发生能量变化的根本原因是化学键的断裂与形成 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |