题目内容
【题目】镁、硫、氮的化合物在工业上用途非常广泛。
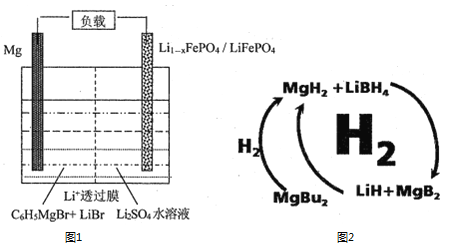
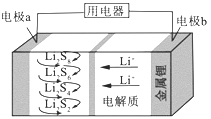
(1)一种镁—锂双离子二次电池的装置如图1所示。
①放电时,Mg电极为_____(填“正极”或“负极”)。
②充电时,Li+迁移至_____________(填“阳极区”或“阴极区”)。
(2)纳米MgH2和LiBH4组成的体系如图2所示,400℃以上受热放氢时发生反应的化学方程式为_____________________________________________。
(3)硝酸厂尾气中含有大量的NO,可用氢气催化还原法除去NO,发生的主要反应如下:
2NO(g)+4H2(g)+O2(g)==N2(g)+4H2O(g) △H =-1143kJ·mol-1
2H2(g)+ O2(g)==2H2O(g) △H =-484kJ·mol-1
则2NO(g)+2H2(g)==N2(g)+2H2O(g) △H =____kJ·mol-1
(4)在一定条件下,反应:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)平衡时CH4的转化率与温度和压强的关系如图3所示。
2CO(g)+2H2(g)平衡时CH4的转化率与温度和压强的关系如图3所示。
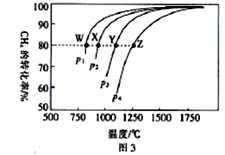
①图中p1、p2、p3、p4代表不同压强,压强最大的是_______。该反应的△H___(填“>”“<”“=”下同)0。
②压强为p4时,在Y点:v(正)__________v(逆)。
③图中W、X、Y、Z四点对应的反应的平衡常数K1、K2、K3、K4由大到小的顺序为______。
【答案】 负极 阴极区 MgH2+2LiBH4![]() 2LiH+MgB2+4H2↑ -659 p4 > < K4>K3>K2>K1
2LiH+MgB2+4H2↑ -659 p4 > < K4>K3>K2>K1
【解析】(1)由镁—锂双离子二次电池的装置图中的信息可知,Mg是负极,Li1-xFePO4是正极。①放电时,Mg电极为负极。②充电时,阳离子向阴极定向移动,所以 Li+迁移至阴极区。
(2)纳米MgH2和LiBH4组成的体系在400℃以上受热放氢时发生反应的化学方程式为MgH2+2LiBH4![]() 2LiH+MgB2+4H2↑ 。
2LiH+MgB2+4H2↑ 。
(3)硝酸厂尾气中含有大量的NO,可用氢气催化还原法除去NO,发生的主要反应如下:①2NO(g)+4H2(g)+O2(g)==N2(g)+4H2O(g) △H =-1143kJ·mol-1;②2H2(g)+ O2(g)==2H2O(g) △H =-484kJ·mol-1。根据盖斯定律,由①-②得,2NO(g)+2H2(g)==N2(g)+2H2O(g) △H =-659kJ·mol-1。
(4)在一定条件下,反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),平衡时CH4的转化率与温度和压强的关系如图3所示。
2CO(g)+2H2(g),平衡时CH4的转化率与温度和压强的关系如图3所示。
①该反应是一个气体分子数增多的反应,在相同温度下, CH4的平衡转化率随压强的增大而减小,所以压强最大的是p4。由图可知,在相同压强下,CH4的平衡转化率随温度的升高而增大,所以该反应为吸热反应,该反应的△H >0。
②由图可知,压强为p4时,在Y点的转化率高于其平衡转化率,所以该反应正在向逆反应方向进行,v(正) <v(逆)。
③由于该反应为吸热反应,所以该反应的平衡常数K随温度升高而增大 ,因此,图中W、X、Y、Z四点对应的反应的平衡常数K1、K2、K3、K4由大到小的顺序为K4>K3>K2>K1。