题目内容
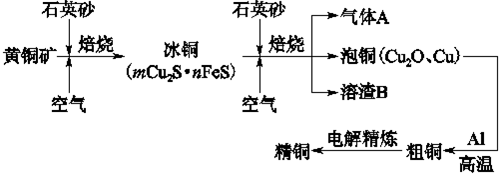
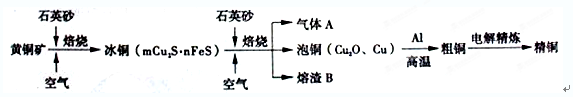
工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
(1)气体A中的大气污染物可选用下列试剂中的
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在
(3)由泡铜(主要成分为Cu2O、Cu)冶炼粗铜的化学反应方程式为

(1)气体A中的大气污染物可选用下列试剂中的
c、d
c、d
吸收.a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在
Fe3+
Fe3+
(填离子符号),检验溶液中还存在Fe2+的方法是取少量溶液,滴加KMnO4溶液,KMnO4褪色,则溶液中存在Fe2+
取少量溶液,滴加KMnO4溶液,KMnO4褪色,则溶液中存在Fe2+
(注明试剂、现象).(3)由泡铜(主要成分为Cu2O、Cu)冶炼粗铜的化学反应方程式为
3Cu2O+2Al
Al2O3+6Cu
| ||
3Cu2O+2Al
Al2O3+6Cu
.
| ||
分析:(1)由流程图转化可知,气体A中的大气污染物主要是二氧化硫,选择试剂吸收二氧化硫,不能产生新的污染气体,二氧化硫是酸性氧化物,结合选项中各物质的性质判断;
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe3+;Fe2+具有还原性,可以利用KMnO4溶液检验;
(3)由流程图转化可知,Cu2O与Al反应置换反应生成Al2O3与Cu;
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe3+;Fe2+具有还原性,可以利用KMnO4溶液检验;
(3)由流程图转化可知,Cu2O与Al反应置换反应生成Al2O3与Cu;
解答:解:(1)由流程图转化可知,气体A中的大气污染物主要是二氧化硫,选择试剂吸收二氧化硫,不能产生新的污染气体,
a.浓H2SO4不能吸收二氧化硫,故a错误;
b.稀HNO3可以吸收二氧化硫,但生成NO污染大气,故b错误;
c.NaOH溶液与二氧化硫反应生成亚硫酸钠和水,不产生新的污染气体,故c正确;
d.氨水与二氧化硫反应生成亚硫酸铵,不产生新的污染气体,故d正确;
故答案为:c、d;
(2)Fe3+遇KSCN溶液变为血红色,用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe3+;Fe2+具有还原性,可以利用KMnO4溶液检验,取少量溶液,滴加KMnO4溶液,KMnO4溶液紫色褪去,
故答案为:Fe3+;取少量溶液,滴加KMnO4溶液,KMnO4溶液紫色褪去,则溶液中存在Fe2+;
(3)由流程图转化可知,Cu2O与Al反应置换反应生成Al2O3与Cu,反应方程式为3Cu2O+2Al
Al2O3+6Cu,
故答案为:3Cu2O+2Al
Al2O3+6Cu;
a.浓H2SO4不能吸收二氧化硫,故a错误;
b.稀HNO3可以吸收二氧化硫,但生成NO污染大气,故b错误;
c.NaOH溶液与二氧化硫反应生成亚硫酸钠和水,不产生新的污染气体,故c正确;
d.氨水与二氧化硫反应生成亚硫酸铵,不产生新的污染气体,故d正确;
故答案为:c、d;
(2)Fe3+遇KSCN溶液变为血红色,用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe3+;Fe2+具有还原性,可以利用KMnO4溶液检验,取少量溶液,滴加KMnO4溶液,KMnO4溶液紫色褪去,
故答案为:Fe3+;取少量溶液,滴加KMnO4溶液,KMnO4溶液紫色褪去,则溶液中存在Fe2+;
(3)由流程图转化可知,Cu2O与Al反应置换反应生成Al2O3与Cu,反应方程式为3Cu2O+2Al
| ||
故答案为:3Cu2O+2Al
| ||
点评:本题考查了元素化合物铜、氮、铁、硫的性质,掌握常见离子的检验是解答本题的关键,题目难度不大.

练习册系列答案
相关题目