题目内容
【题目】下图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336 mL(标准状况)气体。回答:
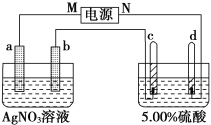
(1)直流电源中,M为________极。
(2)Pt电极上生成的物质是________,其质量为______________________g。
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为2∶________∶________∶________。
(4)AgNO3溶液的浓度________(填“增大”“减小”或“不变”,下同),AgNO3溶液的pH________,硫酸的浓度________,硫酸的pH________。
(5)若硫酸的质量分数由5.00%变为5.02%,则原有5.00%的硫酸________g。
【答案】(1)正 (2)Ag 2.16 (3)2 ![]() 1
1
(4)不变 不变 增大 减小 (5)45.18
【解析】(1)电解5.00%的稀硫酸,实际上是电解其中的水。因此在该电解池中发生反应:2H2O![]() 2H2↑+O2↑,V(H2)∶V(O2)=2∶1。据此可确定d极为阴极,则电源的N极为负极,M极为正极。
2H2↑+O2↑,V(H2)∶V(O2)=2∶1。据此可确定d极为阴极,则电源的N极为负极,M极为正极。
(2)在336 mL气体中,V(H2)=![]() ×336 mL=224 mL,为0.01 mol;V(O2)=
×336 mL=224 mL,为0.01 mol;V(O2)=![]() ×336 mL=112 mL,为0.005 mol。说明电路上有0.02 mol电子转移,因此在b极(Pt、阴极)产生Ag:0.02 mol×108 g·mol1=2.16 g,即0.02 mol的Ag。
×336 mL=112 mL,为0.005 mol。说明电路上有0.02 mol电子转移,因此在b极(Pt、阴极)产生Ag:0.02 mol×108 g·mol1=2.16 g,即0.02 mol的Ag。
(3)n(e)∶n(Ag)∶n(O2)∶n(H2)=0.02∶0.02∶0.005∶0.01=2∶2∶![]() ∶1。
∶1。
(4)由Ag(阳)电极、Pt(阴)电极和AgNO3溶液组成的电镀池,在通电一定时间后,在Pt电极上放电所消耗溶液中Ag+的物质的量等于Ag电极被氧化给溶液补充的Ag+的物质的量,因此AgNO3溶液的浓度不变,溶液的pH也不变。电解5.00%的硫酸溶液,由于其中的水发生电解,因此硫酸浓度增大,由于H+的浓度增大,故溶液的pH减小。
(5)设原5.00%的硫酸为x g,电解时消耗水0.01 mol×18 g·mol1=0.18 g,则:5.00%x=5.02%(x0.18),解得x=45.18 g。

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案