题目内容
【题目】【2017凉山州模拟】如果人体内的CO2不能顺利排除体外会造成酸中毒,缓冲溶液可以抵御外来少量酸或碱对溶液pH的影响,人体血液里主要通过碳酸氢盐缓冲体系(H2CO3/HCO3﹣)维持pH稳定.己知正常人体血液在正常体温时,H2CO3的一级电离常数Ka1=10﹣6,c(HCO3﹣):c(H2CO3)≈20:1,lg2=0.3.
(1)由题给数据可算得正常人体血液的pH (保留一位小数).
(2)正常人体血液中H2CO3、HCO3﹣、OH﹣、H+四种微粒浓度由大到小关系为 ;
(3)当少量的酸、碱进入血液中时,血液pH变化不大,其原因是 。
【答案】(1) 7.4 (2)c(HCO3﹣)>c(H2CO3)>c(OH﹣)>c(H+)
(3)当少量酸进入血液中时,HCO3﹣就与H+发生反应来维持血液的pH稳定,当少量碱进入血液中时,H2CO3就与OH﹣发生反应来维持血液的pH稳定
【解析】(1)Ka=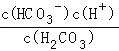 ,Ka=10﹣6.1molL﹣1,正常血液中c(HCO3﹣):c(H2CO3)≈20:1,则c(H+)=10﹣7.4molL﹣1,则pH=7.4;
,Ka=10﹣6.1molL﹣1,正常血液中c(HCO3﹣):c(H2CO3)≈20:1,则c(H+)=10﹣7.4molL﹣1,则pH=7.4;
(2)正常血液中c(HCO3﹣):c(H2CO3)≈20:1,碳酸氢根离子浓度大于碳酸浓度,溶液呈碱性,溶液中离子浓度大小为:c(HCO3﹣)>c(H2CO3)>c(OH﹣)>c(H+);
(3)血液是缓冲溶液,缓冲溶液可以抵御外来少量酸或碱对溶液pH的影响,当少量酸进入血液中时,HCO3﹣就与H+发生反应来维持血液的pH稳定,当少量碱进入血液中时,H2CO3就与OH﹣发生反应来维持血液的pH稳定。

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目