题目内容
【题目】一定温度下,冰醋酸在加水稀释过程中溶液导电能力的变化曲线如图所示,请回答下列问题:
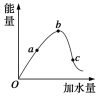
(1)O点导电能力为零的原因是__________________________________。
(2)a、b、c三点中,CH3COOH的电离度最大的是________;CH3COOH的电离平衡常数表达式Ka=________。
(3)若使c点溶液中c(CH3COO-)增大,则下列措施中,可选择________(填字母序号)。
A.加热 B.加入很稀的NaOH溶液
C.加入固体KOH D.加水
E.加入固体CH3COONa F.加入锌粒
(4)在CH3COOH溶液的稀释过程中,始终保持增大趋势的是________(填字母序号)。
A.c(H+) B.H+的个数
C.CH3COOH的分子数 D.c(H+)/c(CH3COOH)
(5)下列有关CH3COOH溶液的说法正确的是________(填字母序号)。
A.CH3COOH溶液中各离子浓度的关系为c(H+)=c(OH-)+c(CH3COO-)
B.向0.10 mol/L的CH3COOH溶液中加水,c(H+)增大
C.CH3COOH溶液中各离子浓度的关系为c(CH3COO-)>c(H+)>c(OH-)
D.常温下,c(H+)=0.01 mol/L的CH3COOH溶液与c(OH-)=0.01 mol/L的NaOH溶液等体积混合后,溶液呈碱性
【答案】(12分,每空2分)
(1)无水醋酸不能电离出离子
(2)c点 c(CH3COO-)·c(H+)/c(CH3COOH)
(3)ACEF
(4)BD (5)A
【解析】(1)O点时冰醋酸中没有水,CH3COOH没有电离,所以此时导电能力为零。(2)在一定温度下,溶液越稀,CH3COOH的电离度越大,因此c点CH3COOH的电离度最大。(3)溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,电离过程吸收热量,加热以及加入固体KOH、加入锌粒均可使平衡正向移动,c(CH3COO-)增大。加入很稀的NaOH溶液、加水虽然也可使平衡正向移动,但因为溶液的体积增大,所以c(CH3COO-)减小。加入固体CH3COONa,平衡逆向移动,但因加入了CH3COO-,故c(CH3COO-)增大。(4)在CH3COOH溶液的稀释过程中,CH3COOH的电离程度增大,因此H+的个数增多。溶液中存在电离平衡:CH3COOH
CH3COO-+H+,电离过程吸收热量,加热以及加入固体KOH、加入锌粒均可使平衡正向移动,c(CH3COO-)增大。加入很稀的NaOH溶液、加水虽然也可使平衡正向移动,但因为溶液的体积增大,所以c(CH3COO-)减小。加入固体CH3COONa,平衡逆向移动,但因加入了CH3COO-,故c(CH3COO-)增大。(4)在CH3COOH溶液的稀释过程中,CH3COOH的电离程度增大,因此H+的个数增多。溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,Ka=c(H+)·c(CH3COO-)/c(CH3COOH),稀释过程中,Ka值不变,c(CH3COO-)减小,故c(H+)/c(CH3COOH)增大。(5)根据溶液中电荷守恒可知,A项正确;稀释虽然使弱酸的电离平衡正向移动,但溶液的酸性减弱,即c(H+)减小,B项错误;CH3COOH溶液中水也发生了微弱电离,所以c(H+)>c(CH3COO-),C项错误;因为CH3COOH只有少部分发生电离,所以反应后CH3COOH过量,溶液呈酸性,D项错误。
CH3COO-+H+,Ka=c(H+)·c(CH3COO-)/c(CH3COOH),稀释过程中,Ka值不变,c(CH3COO-)减小,故c(H+)/c(CH3COOH)增大。(5)根据溶液中电荷守恒可知,A项正确;稀释虽然使弱酸的电离平衡正向移动,但溶液的酸性减弱,即c(H+)减小,B项错误;CH3COOH溶液中水也发生了微弱电离,所以c(H+)>c(CH3COO-),C项错误;因为CH3COOH只有少部分发生电离,所以反应后CH3COOH过量,溶液呈酸性,D项错误。

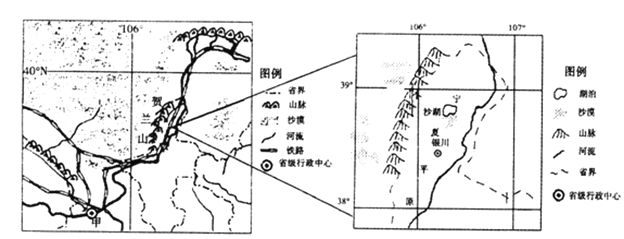
【题目】某校兴趣小组查阅资料时发现,在甲图中①处有一瀑布,有史为证,此瀑布“激流翻滚,惊涛怒吼,其声方圆十里可闻,其形恰如巨壶倒悬,场面极为壮观”。读图回答下列各题。

(1)依据图中信息,说明该瀑布形成的地质作用是________________。该瀑布10万年后
A.①位置上游 | B.①位置下游 | C.保持①位置不变 | D.三种情况都有可能 |
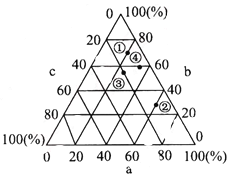
(2)乙图中的岩石按成因属于_______,该类岩石的突出特征是__________________
______________________________________________________。
(3)秋游时,同学们对甲图中②河谷的成因产生了好奇,纷纷发表看法,一共提出了四种假设的成因,请你根据所学的地理知识将下面的假设补充完整。
假设一:向斜,岩层向下弯曲,发育成谷地。
假设二:______________________________________________________。
假设三:______________________________________________________。
假设四:______________________________________________________。
(4)如果要验证上述假设,同学们必须寻找的资料或证据是 。