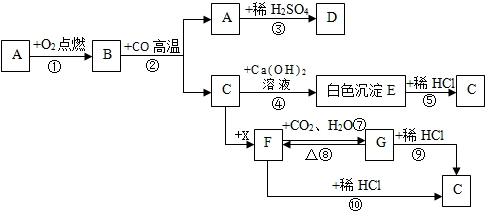
 研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题
进行探究,以下是他们探究的主要过程:
假设:H2O2生成O2的快慢与催化剂种类有关
实验方案:常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间.
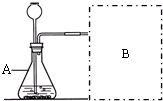
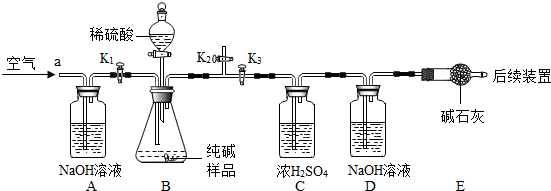
进行实验:如图是他们进行实验的装置图,,此实验中B处宜采用的气体收集方法是:________.
实验记录:
| 实验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g 红砖粉 | 1g MnO2 |
| 时间 | 152s | 35s |
反思:H2O2在常温下分解缓慢,加入MnO2或 红砖粉后反应明显加快,若要证明MnO2和 红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的________和________是否改变.
在一个密闭容器中放入X、Y、Z、Q四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识错误的是
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 20 | 2 | 1 | 37 |
| 反应后质量(g) | 未测 | 32 | 1 | 12 |
- A.物质Z可能是该反应的催化剂
- B.反应后物质X的质量为15g
- C.反应中Y、Q的质量比为6:5
- D.物质Y一定是单质
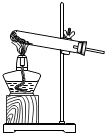
图甲~丁是实验室制取氧气的装置图.
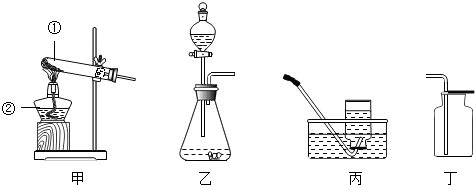
(1)写出仪器的名称:①______、②______.
(2)甲、乙装置都可用于实验室制氧气,用乙装置制氧气的优点是______(填字母).
A.节约能源 B.可较快获得氧气
C.可随时添加药品 D.操作简单、安全
(3)丙、丁装置都可用于实验室收集氧气.下面是对两种收集方法的相关比较(使用容积相同的集气瓶收集氧气).
| 比较的方面 | 排水法 | 向上排气法 | 结论 |
| 方法可行性 | O2难溶于水,且不与水反应. | O2的密度比空气______(填“大”或“小”),且不与空气中的物质发生反应. | 两种方法均可行. |
| 收集O2的纯度 | 分别用排水法和向上排空气法收集两瓶氧气(A和B), 放入两支相同的蜡烛,可观察到B瓶内的蜡烛熄灭较早. 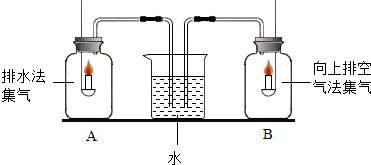 | 结论______. | |
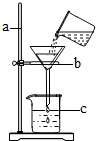
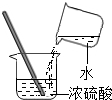
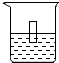
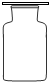 如图所示,这是用排水法收集好的无色气体.就此,请你判断与这种气体相关的物理性质是________.
如图所示,这是用排水法收集好的无色气体.就此,请你判断与这种气体相关的物理性质是________.