��Ŀ����
��������Ҫ�Ļ���ԭ��
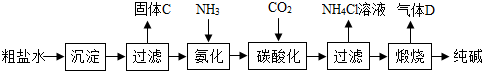
��һ���Ʊ�̽������ͼ�ǹ�ҵ�����������Ҫ����ʾ��ͼ��
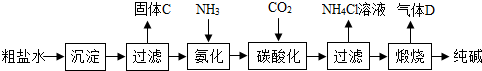
[��������]
�ٴ���ˮ�к�������MgCl2��CaCl2��
�ڳ����£�NH3��������ˮ��CO2������ˮ��
��NaHCO3�����ֽ⣬Na2CO3���Ȳ��ֽ⣮
��1��д����ȥ����ˮ��MgCl2��CaCl2�Ļ�ѧ����ʽ��______��______
��2���ڹ�ҵ��������������У��ȡ���������̼�ữ����Ŀ����______����̼�ữ��ʱ��NaCl��NH3��CO2 ��H2O���������NaHCO3��д���÷�Ӧ�Ļ�ѧ����ʽ______��
��3����̼�ữ������˻�õ�NH4Cl������______�ʣ�Ҳ����______������ȡ�����ȴ����NH4Cl��Һ���ټ�����ʯ�һ��ѭ��ʹ�õ�������______��
��4�������Ƶô���Ļ�ѧ����ʽ��______
�������ɷ�̽��
[�������]������Ʒ�к�����Щ���ʣ�
[����]����һ�����ܺ���NaHCO3�� ����������ܺ���NaCl��
��������______
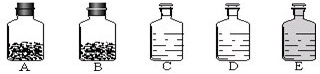
[ʵ��̽��]ȷ���������Ƿ�NaHCO3��ʵ��װ�ú���Ҫʵ�鲽�����£�

�ٳ���D��Eװ��������Ϊ200.0g����10.6 0g��������������ƿ�У�����ͼ��װ�����K1��K2���ر�K3����������һ��ʱ�������
�ڹرջ���K1��K2����K3����������ϡ���ᣬ����ƿ�в��ٲ�������ʱ���ٴδ�ֹˮ��K1���ӵ���a���ٴλ������������
��һ��ʱ����ٴγ���װ��D��E��������Ϊ204.84g��
[ʵ������]
��5��������Ʒǰ��Ӧ______��
��6��װ��A��������______��װ��C��������______��װ��E��������______��
��7����Ӧ�������ֹˮ��K1���������������Ŀ����______��װ��B��һ�������Ļ�ѧ��Ӧ����ʽΪ______װ��D�еĻ�ѧ��Ӧ����ʽΪ______��
��8��װ��B������CO2������Ϊ______ g��ͨ������˵��������______��NaHCO3������ĸ����
A��һ����������B��һ���������� C�����ܡ���������D����ȷ��
������̣���֪Na2CO3��Է�������Ϊ106��NaHCO3��Է�������Ϊ84����______
��9����ȡ10.6��Ʒ������a g 14.6%������ǡ����ȫ��Ӧ���ٽ�������Һ���ɺ�õ����������ΪW����W��ֵ����______����ʱ����Ʒ�к���NaCl��
�⣺��1����ȥ����ˮ��MgCl2��CaCl2�õ��Լ�������������Һ��̼������Һ����Ӧ�Ļ�ѧ����ʽ�ֱ�Ϊ��MgCl2+2NaOH=Mg��OH��2��+2NaCl��CaCl2+Na2CO3=CaCO3��+2Na Cl��
��2���ڹ�ҵ��������������У��ȡ���������̼�ữ����Ŀ������������Һ����CO2���壻�Ȼ��ơ�������������̼��ˮ��Ӧ����̼�����ƺ��Ȼ�泥���Ӧ�Ļ�ѧ����ʽΪ��NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl��
��3����̼�ữ������˻�õ�NH4Cl���е�Ԫ�أ����Կ��������ʣ��Ȼ�鱗��ȶ������ֽ��������ų�������Ҳ���ȼ���NH4Cl��Һ���ټ�����ʯ�һ��ѭ��ʹ�õ�������NH3����������
��4��̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��2NaHCO3 Na2CO3+H2O+CO2����
Na2CO3+H2O+CO2����
����������������Ʒ�л����ܺ���NaHCO3�� NaCl�Ļ���
��5��������Ʒǰ��Ӧ���װ�������ԣ�
��6�������к��ж�����̼��װ��A�������dz�ȥ�����еĶ�����̼��Ũ����ͼ�ʯ�Ҿ�����ˮ�ԣ�װ��C�������dz�ȥ������̼�е�ˮ��װ��E�����������մ�D�д�����ˮ��
��7����Ӧ�������ֹˮ��K1���������������Ŀ���ǽ����ɵĶ�����̼ȫ���͵�D�У�̼���ƺ����ᷴӦ���������ơ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��Na2CO3+H2SO4=Na2SO4+H2O+CO2��������������Һ�Ͷ�����̼��Ӧ����̼���ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��CO2+2NaOH=Na2CO3+H2O��
��8������D��E���ӵ�����Ϊ������̼��������װ��B������CO2������=204.84g-200.0g=4.84g��
����10.6g��ƷȫΪ̼���ƣ����ɶ�����̼������Ϊx
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 44
10.6g x
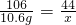
x=4.4g
4.4g��4.84g
������Ʒ�к���̼�����ƣ�
��9������̼���ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼������ȫ����̼����������ӵ�������
Na2CO3+2HCl=2NaCl+H2O+CO2��
73 117
ag��14.6% W

W=0.234ag
���Ե�W��ֵ��������W��0.32aʱ����Ʒ�к���NaCl��
�ʴ�Ϊ����1��MgCl2+2NaOH=Mg��OH��2��+2NaCl��CaCl2+Na2CO3=CaCO3��+2Na Cl��
��2����������Һ����CO2���壻NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl��
��3���������ȣ�NH3����������
��4��2NaHCO3 Na2CO3+H2O+CO2����
Na2CO3+H2O+CO2����
����������NaHCO3�� NaCl��
��5�����װ�������ԣ�
��6����ȥ�����еĶ�����̼�� ��ȥ������̼�е�ˮ�����մ�D�д�����ˮ��
��7�������ɵĶ�����̼ȫ���͵�D�У�Na2CO3+H2SO4=Na2SO4+H2O+CO2����CO2+2NaOH=Na2CO3+H2O��
��8��4.84�� A��
����10.6g��ƷȫΪ̼���ƣ����ɶ�����̼������Ϊx
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 44
10.6g x
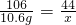
x=4.4g
4.4g��4.84g
������Ʒ�к���̼�����ƣ�
��9��W��0.32a��
��������1�����ݳ�ȥ����ˮ��MgCl2��CaCl2�õ��Լ�������������Һ��̼������Һ���н��
��2�������ڹ�ҵ��������������У��ȡ���������̼�ữ����Ŀ������������Һ����CO2�����Լ��Ȼ��ơ�������������̼��ˮ��Ӧ����̼�����ƺ��Ȼ�什��н��
��3�����ݡ�̼�ữ������˻�õ�NH4Cl���е�Ԫ�ء��Ȼ�鱗��ȶ������ֽ��������ų��������н��
��4������̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼���н��
�������������ݴ�����Ʒ�л����ܺ���NaHCO3�� NaCl���н��
��5�����ݼ�����Ʒǰ��Ӧ���װ�������Խ��н��
��6�����ݿ����к��ж�����̼��װ��A�������dz�ȥ�����еĶ�����̼��Ũ����ͼ�ʯ�Ҿ�����ˮ�Խ��н��
��7�����ݷ�Ӧ�������ֹˮ��K1���������������Ŀ���ǽ����ɵĶ�����̼ȫ���͵�D�С�̼���ƺ����ᷴӦ���������ơ�ˮ�Ͷ�����̼�Լ�����������Һ�Ͷ�����̼��Ӧ����̼���ƺ�ˮ���н��
��8������D��E���ӵ�����Ϊ������̼���������н��
��9������̼���ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼������ȫ����̼����������ӵ��������н��
���������⿼�������ʵ��ᴿ����ѧʵ�����������ʵ�����Ĵ�����֪ʶ���ѶȽϴ�
��2���ڹ�ҵ��������������У��ȡ���������̼�ữ����Ŀ������������Һ����CO2���壻�Ȼ��ơ�������������̼��ˮ��Ӧ����̼�����ƺ��Ȼ�泥���Ӧ�Ļ�ѧ����ʽΪ��NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl��
��3����̼�ữ������˻�õ�NH4Cl���е�Ԫ�أ����Կ��������ʣ��Ȼ�鱗��ȶ������ֽ��������ų�������Ҳ���ȼ���NH4Cl��Һ���ټ�����ʯ�һ��ѭ��ʹ�õ�������NH3����������
��4��̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��2NaHCO3
 Na2CO3+H2O+CO2����
Na2CO3+H2O+CO2��������������������Ʒ�л����ܺ���NaHCO3�� NaCl�Ļ���
��5��������Ʒǰ��Ӧ���װ�������ԣ�
��6�������к��ж�����̼��װ��A�������dz�ȥ�����еĶ�����̼��Ũ����ͼ�ʯ�Ҿ�����ˮ�ԣ�װ��C�������dz�ȥ������̼�е�ˮ��װ��E�����������մ�D�д�����ˮ��
��7����Ӧ�������ֹˮ��K1���������������Ŀ���ǽ����ɵĶ�����̼ȫ���͵�D�У�̼���ƺ����ᷴӦ���������ơ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��Na2CO3+H2SO4=Na2SO4+H2O+CO2��������������Һ�Ͷ�����̼��Ӧ����̼���ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��CO2+2NaOH=Na2CO3+H2O��
��8������D��E���ӵ�����Ϊ������̼��������װ��B������CO2������=204.84g-200.0g=4.84g��
����10.6g��ƷȫΪ̼���ƣ����ɶ�����̼������Ϊx
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 44
10.6g x
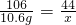
x=4.4g
4.4g��4.84g
������Ʒ�к���̼�����ƣ�
��9������̼���ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼������ȫ����̼����������ӵ�������
Na2CO3+2HCl=2NaCl+H2O+CO2��
73 117
ag��14.6% W

W=0.234ag
���Ե�W��ֵ��������W��0.32aʱ����Ʒ�к���NaCl��
�ʴ�Ϊ����1��MgCl2+2NaOH=Mg��OH��2��+2NaCl��CaCl2+Na2CO3=CaCO3��+2Na Cl��
��2����������Һ����CO2���壻NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl��
��3���������ȣ�NH3����������
��4��2NaHCO3
 Na2CO3+H2O+CO2����
Na2CO3+H2O+CO2��������������NaHCO3�� NaCl��
��5�����װ�������ԣ�
��6����ȥ�����еĶ�����̼�� ��ȥ������̼�е�ˮ�����մ�D�д�����ˮ��
��7�������ɵĶ�����̼ȫ���͵�D�У�Na2CO3+H2SO4=Na2SO4+H2O+CO2����CO2+2NaOH=Na2CO3+H2O��
��8��4.84�� A��
����10.6g��ƷȫΪ̼���ƣ����ɶ�����̼������Ϊx
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 44
10.6g x
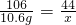
x=4.4g
4.4g��4.84g
������Ʒ�к���̼�����ƣ�
��9��W��0.32a��
��������1�����ݳ�ȥ����ˮ��MgCl2��CaCl2�õ��Լ�������������Һ��̼������Һ���н��
��2�������ڹ�ҵ��������������У��ȡ���������̼�ữ����Ŀ������������Һ����CO2�����Լ��Ȼ��ơ�������������̼��ˮ��Ӧ����̼�����ƺ��Ȼ�什��н��
��3�����ݡ�̼�ữ������˻�õ�NH4Cl���е�Ԫ�ء��Ȼ�鱗��ȶ������ֽ��������ų��������н��
��4������̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼���н��
�������������ݴ�����Ʒ�л����ܺ���NaHCO3�� NaCl���н��
��5�����ݼ�����Ʒǰ��Ӧ���װ�������Խ��н��
��6�����ݿ����к��ж�����̼��װ��A�������dz�ȥ�����еĶ�����̼��Ũ����ͼ�ʯ�Ҿ�����ˮ�Խ��н��
��7�����ݷ�Ӧ�������ֹˮ��K1���������������Ŀ���ǽ����ɵĶ�����̼ȫ���͵�D�С�̼���ƺ����ᷴӦ���������ơ�ˮ�Ͷ�����̼�Լ�����������Һ�Ͷ�����̼��Ӧ����̼���ƺ�ˮ���н��
��8������D��E���ӵ�����Ϊ������̼���������н��
��9������̼���ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼������ȫ����̼����������ӵ��������н��
���������⿼�������ʵ��ᴿ����ѧʵ�����������ʵ�����Ĵ�����֪ʶ���ѶȽϴ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ