(7分)某同学设计下表所示实验,探究金属铜对H2O2分解速率的影响。
|
操作 |
装置 |
|
|
1、取一小块铜丝网,卷成筒形,固定在铜丝上。 |
|
|
|
2、分别向①和②中注入15mL、30%的H2O2,并放入盛有热水的③中。 |
|
约1min后可观察到① 和②中都有少量气泡产生
|
|
3、把铜丝插入①中。 |
|
①中有大量气泡产生,约5min后不再有气泡产生;此时②中 仍然有少量气泡产生
|
回答下列问题:
(1)仪器的①名称是______________,仪器③的名称是______________;
(2)仪器②中实验的目的是 ;
(3)根据上述实验,可以得出的结论是 ;
(4)如果用本实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是________。
A.称量实验前铜丝网的质量
B.将实验后的铜丝网干燥、称重
C.向仪器中加入二氧化锰
D.将实验后的铜丝网插入AgNO3溶液中
(12分)实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气。
(1)查阅资料。
20℃时不同质量分数硫酸的密度(g/mL)
|
质量 分数 |
0% (纯水) |
1% |
4% |
10% |
16% |
24% |
32% |
36% |
44% |
49% |
60% |
98% |
|
密度 |
1.00 |
1.01 |
1.02 |
1.07 |
1.11 |
1.17 |
1.24 |
1.27 |
1.34 |
1.39 |
1.50 |
1.84 |
分析以上数据,可以得出结论(写2条)
① ;
② ;
(2)计算。配制200g24.5%的稀硫酸,需 g98%浓硫酸和 g水。实际操作时,取98%浓硫酸 mL(精确到1mL);
(3)配制稀硫酸。分别用量筒量取所需水和浓硫酸,先将 倒入烧杯中,然后
;
(4)制取氢气。
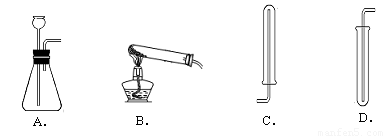
①下图中可用于制取、收集氢气的装置是(填字母) ;
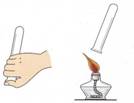
②检验氢气纯度的方法如图所示,标明氢气不纯的现象是 。
请你和小明一起进行实验室制取二氧化碳的探究。
(1)选择药品。小明对三组药品进行了研究,实验记录如下:
|
组别 |
药品 |
实验现象 |
|
① |
块状石灰石和稀盐酸 |
产生气泡速率适中 |
|
② |
块状石灰石和稀硫酸 |
产生气泡速率缓慢并逐渐停止 |
|
③ |
碳酸钠粉末和稀盐酸 |
产生气泡速率很快 |
从制取和收集的角度分析,一般选择第①组药品,该组药品发生反应的化学方程式
为 ;
不选择第③组药品的原因是 。
(2)选择装置。通过对制取氧气装置的分析,他选择用过氧化氢制取氧气的发生装置。你认为他选择的依据是 。
(3)制取气体。将药品装入所选装置制取气体,并用向上排空气法收集。
验满方法是 。
(4)气体检验。将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳。他的检验方法是否正确?请说明理由。
。
 现象
现象






