浴室喷头长时间使用会有白色固体附着,这是因为硬水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙[Ca(HCO3)2]受热易分解,生成难溶性的化合物、气体等物质.某小组探究碳酸氢钙受热分解后产物的成分.
【提出猜想】从组成物质元素的角度分析:
猜想1.生成的难溶性化合物可能是碳酸钙.
猜想2.放出的气体可能是CO2、________、________等.
【方案设计】请你设计实验,帮助该组同学确定难溶物的成分.
| 实验步骤 | 实验现象和结论 |
| ________ | ________: 则证明难溶物为碳酸钙 |
操作1.加热A装置,一段时间后,B装置中的澄清石灰水变浑浊.
操作2.在a处用燃着的木条检验,无明显现象.
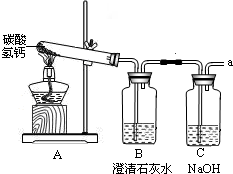
【实验结论】
结论1.碳酸氢钙分解产生的气体一定有CO2;一定没有________.
结论2.碳酸氢钙受热分解的化学方程式为Ca(HCO3)2
 CaCO3↓+CO2↑+H2O
CaCO3↓+CO2↑+H2O【实验交流】
交流1.从安全的角度考虑,实验操作2中存在的不足是________.
交流2.小组内某同学对上述结论提出异议:
| 该同学的观点 | 请说出你的观点并阐述理由 |
| 该实验没有对氧气进行验证 | |
| “结论2”不正确 |
根据所给信息,在横线处填上相应物质的名称或化学式:
(1).地球表面约71%被它覆盖,常用作化学实验的溶剂的物质是______;
(2).孔雀石中所含的元素、湿法冶金的产物、电的良导体.它是______.
 在实验探究课上,老师给了同学们一包红色粉末,该粉末是铜粉和氧化铁(Fe2O3)粉末中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究活动并回答问题.
在实验探究课上,老师给了同学们一包红色粉末,该粉末是铜粉和氧化铁(Fe2O3)粉末中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究活动并回答问题.
(1)[提出问题]假设1:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;假设3:红色粉末是______.
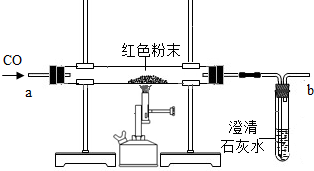
(2)[设计实验方案]同学们为了验证上述假设,设计了如下图所示实验装置,并对实验结果作了如下设想和分析:取少量红色粉末放人硬质玻璃管中,通入一氧化碳,片刻后加热至充分反应.
请你完成下表:
| 实验中可能出现的现象 | 结论 |
| 则假设1成立 | |
| 则假设2成立 | |
| 则假设3成立 |
(4)[反思与评价]
(1)实验过程中,硬质玻璃管内发生反应的化学方程式是:______.
(2)用化学方程式表示实验过程中石灰水发生的变化:______.
(3)从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是______.
 小华是个非常爱动脑的同学,做溶液的导电性实验时,小华观察得非常仔细,以下是他们小组观察、记录并思考的一些问题:
小华是个非常爱动脑的同学,做溶液的导电性实验时,小华观察得非常仔细,以下是他们小组观察、记录并思考的一些问题:
(1)电解水时,通常要加入少量氢氧化钠溶液或稀硫酸,目的是______.
(2)经过溶液的学习后,小华明白了不是所有的溶液都能导电的道理,下列物质加入水中充分振荡后能导电的是______.
A.蔗糖 B.植物油 C.高锰酸钾 D.碳酸钠
(3)做氯化钠溶液的导电性实验时,小华不仅看到灯泡亮了,还观察到与电解水相似的现象:两根石墨电极上都出现了气泡.这激发了小华探究气泡成分的欲望.请你一起参与小华的探究活动吧!
[提出问题]氯化钠溶液通电时石墨电极上分别生成了什么气体?
[查阅资料]Cl2是黄绿色、有刺激性气味的有毒气体,常温下1体积水能溶解2体积Cl2.
[提出假设]假设1:电极上分别生成了氢气和氯气;
假设2:电极上分别生成了氧气和氯气;
假设3:电极上分别生成了氢气和氧气.以上假设的依据是______.
[设计实验]小华决定用右图所示的装置来电解氯化钠的饱和溶液.并收集两个电极上产生的气体.
[实验分析]观察到一支试管中收集的气体为黄绿色,另一支试管中收集到的气体能被点燃,则假设______成立:小红又向反应后的溶液中滴加无色酚酞,结果酚酞变红,请写出氯化钠溶液通电时发生反应的化学方程式_______.
[反思与评价]联想电解水的实验,你认为在电解水时______(填“可以”或“不可以”)加入少量的氯化钠溶液,原因是______.
(4)小华还想利用H2还原氧化铁的实验测定水中氢、氧两种元素的质量比.
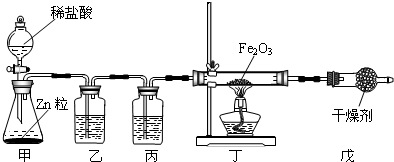
[设计实验]实验装置图如下:
①写出装置中试剂的名称:乙______,丙______.
②实验开始时,应该先______(选填字母).
a.加热反应管丁 b.从分液漏斗中滴加液体
在这两步操作之间,还应进行的一步操作是______.
③写出反应管丁中发生反应的化学方程式:______.
[进行实验]该小组同学进行了实验,测得了下列数据:
| 反应前 | 反应后 | |
| 丁管和内盛物的总质量 | 132.4g | 130.0g(冷却到室温称量) |
| 戊管及内盛物的总质量 | 143.2g | 145.9g |
[误差分析]
①如果该实验缺少装置丙,则测得的水中氢、氧两种元素的质量比会______(选填“偏大”或“偏小”).
②如果实验后观察到反应管丁中有水珠凝结,则测得的水中氢、氧两种元素的质量比会______(选填“偏大”或“偏小”).
氢氧化钠固体及溶液在空气中很容易发生变质生成碳酸钠.
(1)甲同学在实验室里发现一瓶敞口放置的氢氧化钠溶液,对其变质情况进行了如下探究.
【猜想与假设】该氢氧化钠溶液已部分变质.
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量该溶液于一支试管中,加入______ | ______ | 该氢氧化钠溶液已变质 |
| b.将步骤a所得的液体静置,取上层清液于另一支试管中,滴加______ | ______ | 该氢氧化钠溶液已部分变质 |
向该溶液中加入______,充分反应后即可除去该氢氧化钠溶液中含有的杂质.
(2)乙同学在实验室里发现少量部分变质的氢氧化钠固体,尝试通过实验测定其中碳酸钠的质量分数.
【设计和进行实验】乙同学设计了下图所示的实验装置(铁架台、铁夹等固定用装置已略去,碱石灰是固体氢氧化钠和生石灰的混合物).取10.0g待测样品,进行实验.
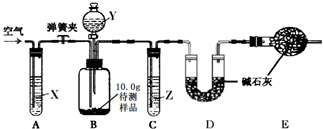
实验步骤如下:
a.连接好装置,并检查气密性; b.打开弹簧夹,缓缓通入一段时间空气;
c.称量装置D的质量为83.4g; d.关闭弹簧夹,慢慢滴加Y溶液,至不再产生气泡为止;
e.打开弹簧夹,再次缓缓通入一段时间空气; f.再次称量装置D的质量为84.5g.
【交流讨论】
①试剂X、Y、Z依次最适宜选用______(选填字母).
A.氢氧化钠溶液 浓盐酸 浓硫酸 B.澄清石灰水 稀盐酸 稀硫酸
C.氢氧化钠溶液 稀硫酸 浓硫酸 D.浓硫酸 稀硫酸 氢氧化钠溶液
②步骤e中通入空气的作用是______.
③若没有装置C,则会导致测定结果______(选填“偏大”、“偏小”或“无影响”).
填写下列空白
| 化学符号 | ________ | 2Na | ________ | ________ | ________ |
| 化学含义 | 3个氢分子 | ________ | +3价的铝元素 | 三个氖原子 | 两个亚铁离子 |