(7分)根据实验内容回答问题。
|
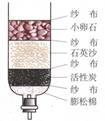
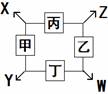
实验装置图 |
Ⅰ.通入CO2 Ⅱ.加热 |
Ⅲ |
Ⅳ Ⅴ |
|
现象及问题 |
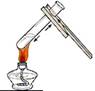
实验Ⅰ是向紫色石蕊溶液中通入CO2,该实验使紫色石蕊溶液变红的物质为 。 实验Ⅱ是将实验Ⅰ中所得混合液加热,实验现象为 ,发生反应的化学方程式为 。 |
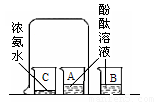
实验Ⅲ的现象是 ,此实验说明了(填序号) 。 ①氨分子不断运动 ②酚酞分子不运动 ③氨水呈碱性 ④氨水易挥发 |
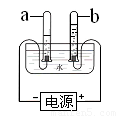
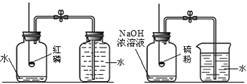
实验Ⅳ和Ⅴ装置中,能完成测定空气中氧气体积分数的是(填序号) 。红磷燃烧的化学反应方程式为 。 |
(3分)黄铜是由铜和锌所组成的合金,用途广泛。某兴趣小组为探究黄铜合金的组成,取20.00 g粉末状黄铜合金样品,把60.00 g稀硫酸平均分成三等份,分三次加入样品中,均有气体产生,充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
|
|
第一次 |
第二次 |
第三次 |
|
剩余固体的质量/g |
16.75 |
13.50 |
12.40 |
请计算:(要求写出计算过程)
(1)该黄铜合金中,锌元素的质量分数。
(2)第二次实验中放出气体的质量。
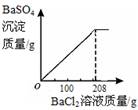
(3)向三次实验后所得混合溶液中滴加BaCl2溶液,生成不溶于水的BaSO4白色沉淀。所得沉淀的质量与BaCl2溶液质量的关系如右图所示,求所用BaCl2溶液的溶质质量分数。