先在表中空白处填写相关的内容,再根据表中提供的信息研究下面的问题.
| 反应物I | 反应物Ⅱ | 反应现象 | 说 明 |
| AgNO3溶液 | NaCl溶液 | 生成白色沉淀 | 该沉淀为AgCl,不溶于稀HNO3 |
| BaCl2溶液 | Na2SO4溶液 | 生成白色沉淀 | 该沉淀为BaSO4,不溶于稀HCl |
| Na2CO3溶液 | ______ | 生成白色沉淀 | 该沉淀为______,溶于稀HCl |
问:
(1)Na2SO4和CaCl2在溶液里能形成K+、SO42-、Ca2+和Cl-四种离子.要除去其中的Ca2+,可使用______溶液;
除去其中的SO42-,可使用______溶液.
(2)在工业生产的除杂过程中,又会带进CO32-和OH-.要同时除去这两种杂质离子,最简便的方法是加入适量的______,
并用______测定溶液的酸碱性.
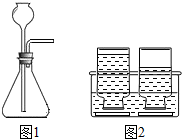
在基础实验课上,教师将某班组同学分为A、B两大组,进行了CO2的制备(利用图1装置)、收集方法及有关CO2的性质实验的研究.
I.实验原理、步骤及现象:
| 实验步骤 | 实验原理、操作及现象 |
| (1)连接仪器 | |
| (2)检查装置的气密性 | ______ |
| (3)加药品:先向250mL锥形瓶中加入颗粒大小差不多的石灰石10块,旋紧橡胶塞后再从长颈漏斗中加盐酸(1:2)25mL | 反应的化学方程式:______ |
| (4)收集:A组用排水法,B组用向上排空气法,各收集两瓶(250mL)CO2,并记录收集满第一瓶的时间(从倒盐酸时开始计时).正放桌面上备用. | A组观察到______现象时,表明气体已经收集满.B组的验满方法及现象是______记录集满第一瓶气体所需要的时间. |
(5)将收集到的两瓶气体分别慢慢倒入放有燃着的蜡烛的烧杯中,如图所示,观察现象.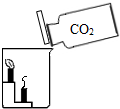 | ______ |
| 分工 | A大组(排水法) | B大组(向上排空气法) | ||||||
| 第一组 | 第二组 | 第三组 | 第四组 | 第一组 | 第二组 | 第三组 | 第四组 | |
| 集满气体时间 | 35″ | 43″ | 39″ | 44″3 | 1′15″ | 1′4″ | 1′12″ | 59″ |
(1)完成表格中的空白之处.
(2)分析实验记录的时间后发现:集满一瓶气体所用时间排水法比向上排空气法______(填“长”或“短”).
(3)A大组同学在进行第5步性质实验时,发现第一瓶气体倾倒入烧杯中,燃着蜡烛均未熄灭,而第二瓶气体倾倒入烧杯中,燃着的蜡烛均熄灭了,可能的原因:______.
Ⅳ.实验延伸:
老师将不同收集方法得到的第二瓶气体倒放入NaOH溶液中(NaOH溶液可以吸收CO2,反应原理是CO2+2NaOH=Na2CO3+H2O),如图2所示,一段时间后发现:集气瓶内液面均上升,上升高度:排水法明显高于向上排空气法可能的原因是:______.
V.实验结论:CO2能用排水法收集理由是:______.