(2010?无锡)一定条件下,在一个密闭容器中发生某反应.测得反应过程中各物质的质量如下表所示
下列判断错误的是( )
| 物 质 | X | Y | Z | Q |
| 第一次测得的质量/g | 68 | 16 | 4.4 | 3.6 |
| 第二次测得的质量/g | 4 | 未测 | 48.4 | 39.6 |
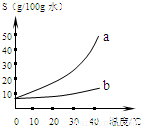
(2011?闵行区一模)以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
(1)Na2CO3溶解度曲线为(填“a”或“b”).
(2)要除去Na2CO3固体中的少量NaHCO3,应采用的物理方法是(填写编号).
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是.
(4)40℃时的100g Na2CO3的饱和溶液中含有g溶质,该溶液的溶质质量分数为%.(计算结果精确到0.1)
(5)若将30%的碳酸钠溶液100g,稀释到10%,需要加水mL.
0 89725 89733 89739 89743 89749 89751 89755 89761 89763 89769 89775 89779 89781 89785 89791 89793 89799 89803 89805 89809 89811 89815 89817 89819 89820 89821 89823 89824 89825 89827 89829 89833 89835 89839 89841 89845 89851 89853 89859 89863 89865 89869 89875 89881 89883 89889 89893 89895 89901 89905 89911 89919 211419
(1)Na2CO3溶解度曲线为(填“a”或“b”).
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是.
(4)40℃时的100g Na2CO3的饱和溶液中含有g溶质,该溶液的溶质质量分数为%.(计算结果精确到0.1)
(5)若将30%的碳酸钠溶液100g,稀释到10%,需要加水mL.

 (2011?闵行区一模)t℃时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成下图中的斜线.下列说法正确的是( )
(2011?闵行区一模)t℃时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成下图中的斜线.下列说法正确的是( )
