
(I)图(1)是 A、B、C三种固体物质的溶解度曲线.
请回答:
(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 ;
(2)当温度从t2℃降到t1℃时,三物质的饱和溶液中没有晶体析出的是 .
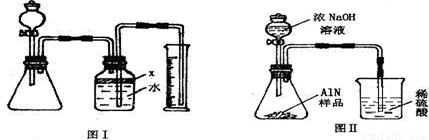
(II)用图(2)中的装置可进行气体和固体的反应.
(1)请在下表中写出两组不同的反应物(两组气体必须各不相同).
| 组别 | 固 体 | 气 体 |
| 1 | ||
| 2 |
(1)高中教材中有这样一个实验:在两支试管中分别加入3mL(足量)稀盐酸,将两个各装有0.3g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.(已知:Na2CO3与稀盐酸时先发生:Na2CO3+HCl=NaCl+NaHCO3,然后NaHCO3发生:NaHCO3+HCl=NaCl+H2O+CO2↑)当将气球内的NaHCO3或Na2CO3粉末同时倒入试管中,观察到现象如下:
①试管中(填产生沉淀或气体及反应速率等相关现象) .
②盛 的试管中气球变得更大,大小气球(包含试管)体积之比约为(填最简整数比) ;
③等质量的两种固体完全反应后生成气体质量不等,但等质量的稀盐酸完全反应后生成气体质量相等,这个结论正确吗?
④综上所述,在泡沫灭火器中常选用 来产生CO2(选填NaHCO3或Na2CO3)
(2)为研究是吸热还是放热反应,继续进行了下列实验(每个实验各做3次,取平均值):
请你帮助填写相关内容:
①该研究报告的题目是《 》
②该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为 和 ;通过上述实验可得出四条结论:
a:NaHCO3 的溶解是 (吸热或放热)过程;
b:Na2CO3 溶解是 (吸热或放热)过程;
c:NaHCO3的饱和溶液和盐酸的反应是 (吸热或放热)反应;
d:Na2CO3的饱和溶液和盐酸的反应是 (吸热或放热)反应.

0 84010 84018 84024 84028 84034 84036 84040 84046 84048 84054 84060 84064 84066 84070 84076 84078 84084 84088 84090 84094 84096 84100 84102 84104 84105 84106 84108 84109 84110 84112 84114 84118 84120 84124 84126 84130 84136 84138 84144 84148 84150 84154 84160 84166 84168 84174 84178 84180 84186 84190 84196 84204 211419
①试管中(填产生沉淀或气体及反应速率等相关现象) .
②盛 的试管中气球变得更大,大小气球(包含试管)体积之比约为(填最简整数比) ;
③等质量的两种固体完全反应后生成气体质量不等,但等质量的稀盐酸完全反应后生成气体质量相等,这个结论正确吗?
④综上所述,在泡沫灭火器中常选用 来产生CO2(选填NaHCO3或Na2CO3)
(2)为研究是吸热还是放热反应,继续进行了下列实验(每个实验各做3次,取平均值):
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高或最低温度 |
| ① | 35mL水 | 2.5gNaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL水 | 2.5g Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 35mL稀盐酸 | 含2.5g NaHCO3的饱和溶液32.5mL | 20℃ | 19℃ |
| ④ | 35mL稀盐酸 | 含3.2g Na2CO3的饱和溶液23.1mL+10mL水 | 20℃ | 24.2℃ |
| ⑤ | 35mL稀盐酸 | 2.5g NaHCO3固体 | 20℃ | 16.2℃ |
| ⑥ | 35mL稀盐酸 | 2.5g Na2CO3固体 | 20℃ | 25.1℃ |
①该研究报告的题目是《 》
②该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为 和 ;通过上述实验可得出四条结论:
a:NaHCO3 的溶解是 (吸热或放热)过程;
b:Na2CO3 溶解是 (吸热或放热)过程;
c:NaHCO3的饱和溶液和盐酸的反应是 (吸热或放热)反应;
d:Na2CO3的饱和溶液和盐酸的反应是 (吸热或放热)反应.

 4Fe+3CO2↑或者为:Fe2O3+3C
4Fe+3CO2↑或者为:Fe2O3+3C 2Fe+3CO↑
2Fe+3CO↑ 4FeO十CO2↑,为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入碳多少克? .
4FeO十CO2↑,为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入碳多少克? .
 火箭发射
火箭发射

