20℃时,NaCl溶解于水的实验数据如图.则下列叙述正确的是( )
A.②中所得溶液是饱和溶液
B.20℃时10g水最多能溶解4gNaCl
C.③④溶液的溶质质量分数相等
D.①所得溶液的溶质质量分数为20%
| 实验序号 | 水的质量(g) | 加入NaCl的质量(g) | 溶液的质量(g) |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | 13.6 |
A.②中所得溶液是饱和溶液
B.20℃时10g水最多能溶解4gNaCl
C.③④溶液的溶质质量分数相等
D.①所得溶液的溶质质量分数为20%
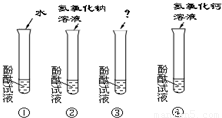
下列是分析已变质氢氧化钠溶液的相关实验,其中合理的是( )
A.②③
B.①③
C.②④
D.①④
| 序号 | 实验目的 | 实验过程 |
| ① | 除去杂质 | 取溶液,滴加石灰水至恰好完全反应,过滤 |
| ② | 确定成分 | 取少量溶液,加入石灰水,过滤,向滤液中滴加酚酞溶液 |
| ③ | 证明变质 | 取少量溶液,滴加盐酸,将生成的气体通入澄清的石灰水 |
| ④ | 测定纯度 | 取一定量溶液,加入盐酸,用氢氧化钠固体吸收气体,称量 |
A.②③
B.①③
C.②④
D.①④
天然水中含有的部分杂质如下表所示:
请根据上表内容回答:
(1)写出“主要气体”中两种气体的化学式______、______;
(2)写出“主要离子”中一种阳离子和一种阴离子的符号______、______;
(3)写出由“生物生成物”中的离子组成的磷酸二氢铵的化学式______.
| 溶 解 物 质 | 悬浮物质 | ||
| 主要气体 | 主要离子 | 生物生成物 | 细菌、藻类及原生 物、泥沙、黏土等 |
| 氧气 二氧化碳 硫化氢等 | 钙离子、氯离子、 硫酸根离子 镁离子 | NH4+、NO2-、 HPO42-、Fe3+、 H2PO4-等 | |
(1)写出“主要气体”中两种气体的化学式______、______;
(2)写出“主要离子”中一种阳离子和一种阴离子的符号______、______;
(3)写出由“生物生成物”中的离子组成的磷酸二氢铵的化学式______.
图1是实验室制备某些常见气体的装置示意图.
(1)实验室制备CO2的化学方程式为 可用的发生装置是 (选填图1字母序号).
(2)排水法收集与排空气法收集CO2的比较
(3)块状石灰石(杂质不溶于水,也不与盐酸反应)和适量稀盐酸反应至气泡逸出不明显后,测得其残留液pH等于2.此时取适量反应后溶液,逐滴滴入碳酸钠溶液,并用pH数字探测仪连续监测,得曲线如图2[pH为纵坐标,时间s(秒)为横坐标]:
①在AB段实验的现象是 ,产生该现象的化学方程式为 ,②BC“平台”段实验的现象是 ,产生该现象的化学方程式为 .③CD段上升说明碳酸钠溶液已经 .进行到D点时,溶液中所含溶质是 .
0 83827 83835 83841 83845 83851 83853 83857 83863 83865 83871 83877 83881 83883 83887 83893 83895 83901 83905 83907 83911 83913 83917 83919 83921 83922 83923 83925 83926 83927 83929 83931 83935 83937 83941 83943 83947 83953 83955 83961 83965 83967 83971 83977 83983 83985 83991 83995 83997 84003 84007 84013 84021 211419

(1)实验室制备CO2的化学方程式为 可用的发生装置是 (选填图1字母序号).
(2)排水法收集与排空气法收集CO2的比较
| 比较项目 | 排水法 | 向上排空气法 |
| 收集方法可行性分析 | CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率 | CO2不与空气中主要成分反应,且 |
| 收集验满过程分析 | 集满的现象是:集气瓶内液面降至瓶口,且有 从瓶口逸出 | 集满的现象是:用燃烧的木条放在瓶口,燃烧的木条 |
①在AB段实验的现象是 ,产生该现象的化学方程式为 ,②BC“平台”段实验的现象是 ,产生该现象的化学方程式为 .③CD段上升说明碳酸钠溶液已经 .进行到D点时,溶液中所含溶质是 .
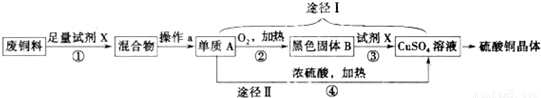
 CuSO4+SO2↑+2H2O.从经济和环保的角度分析,对比途径I、Ⅱ,途径I的优点有:获得等量硫酸铜消耗的硫酸少和 .
CuSO4+SO2↑+2H2O.从经济和环保的角度分析,对比途径I、Ⅱ,途径I的优点有:获得等量硫酸铜消耗的硫酸少和 .