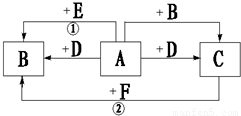
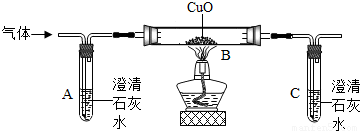
化学兴趣小组的同学对实验室一瓶久置的NaOH固体进行了实验探究.
提出问题:这瓶NaOH固体是否变质,变质情况怎么样?
猜想:①:没变质,全部是NaOH;
猜想②:部分变质,既含有NaOH又含有Na2CO3;
猜想③:完全变质,全部是Na2CO3.
查阅资料:部分盐溶液在常温下的pH如下表:
设计并完成实验
反思:上述步骤①中滴加过量CaCl2溶液的目的是______,判断CaCl2溶液是否过量的方法是______;
拓展:如果要确定该样品的变质程度,则需要测定的两组数据是(假定试剂中无其它杂质)______.
提出问题:这瓶NaOH固体是否变质,变质情况怎么样?
猜想:①:没变质,全部是NaOH;
猜想②:部分变质,既含有NaOH又含有Na2CO3;
猜想③:完全变质,全部是Na2CO3.
查阅资料:部分盐溶液在常温下的pH如下表:
| 盐溶液 | NaCl | Na2CO3 | CaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样品溶于水配成溶液,向溶液中滴加CaCl2溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中一定含有______(填化学式,下同). |
| ②用玻璃棒蘸取少量①的上层清液滴在pH试纸上,与标准比色卡对照. | pH=11 | 说明上述猜想中______是正确的. |
拓展:如果要确定该样品的变质程度,则需要测定的两组数据是(假定试剂中无其它杂质)______.
某化学兴趣小组的同学对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所用的稀硫酸与铁样品恰好完全反应.实验数据如下表:
(1)______同学所用的稀硫酸与铁样品恰好完全反应;共产生______g气体.
(2)计算样品中的铁的质量分数是多少?
(3)计算恰好完全反应后所得溶液中溶质的质量分数?(烧杯质量为25.4克)
0 83604 83612 83618 83622 83628 83630 83634 83640 83642 83648 83654 83658 83660 83664 83670 83672 83678 83682 83684 83688 83690 83694 83696 83698 83699 83700 83702 83703 83704 83706 83708 83712 83714 83718 83720 83724 83730 83732 83738 83742 83744 83748 83754 83760 83762 83768 83772 83774 83780 83784 83790 83798 211419
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的铁样品 | 9g | 9g | 14g |
| 充分反应后,烧杯+剩余物 | 208.7g | 158.7g | 163.7g |
(2)计算样品中的铁的质量分数是多少?
(3)计算恰好完全反应后所得溶液中溶质的质量分数?(烧杯质量为25.4克)