通过近一年的化学实验探究,小林发现金属和酸反应生成氢气的速率与金属的状态、酸的浓度、反应的温度等条件有关.下表是他对铝与稀盐酸反应受哪些条件的影响的探究(其中铝和稀盐酸每次的用量都相同).请你根据表中的信息填空:
(1)写出铝与稀盐酸反应的化学方程式 .
(2)用②和③来探究铝的状态对反应速率的影响,小林进行实验③时的温度为 ;
(3)要探究温度对反应速率的影响,小林设计的实验组合是 (填写实验编号);
(4)小林设计实验组合①②的目的是 ;
(5)实验探究时,小林每次收集的氢气均为30mL,则实验中他还应记录的实验数据是 ;
(6)在进行上述铝与稀盐酸反应时,粗心的小林不小心将氢氧化钠溶液倒入了铝片中,发现也有气泡产生,好奇的他继续进行了如下实验探究:
【提出问题】铝与氢氧化钠溶液反应时生成的气体是什么?
【进行猜想】猜想①:可能是CO2;猜想②:可能是O2;猜想③:可能是H2.
你认为猜想 是不合理的,理由是 ;
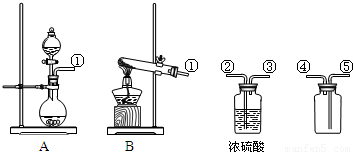
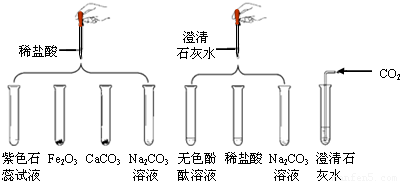
【实验方案】①收集气体:实验时气体收集的方法是 ;
②检验气体:验证猜想②的方法是 ;
【得出结论】铝与氢氧化钠溶液反应的方程式为:
2Al+2NaOH+2H2O=2 +3H2↑(在横线上填上化学式).
0 83546 83554 83560 83564 83570 83572 83576 83582 83584 83590 83596 83600 83602 83606 83612 83614 83620 83624 83626 83630 83632 83636 83638 83640 83641 83642 83644 83645 83646 83648 83650 83654 83656 83660 83662 83666 83672 83674 83680 83684 83686 83690 83696 83702 83704 83710 83714 83716 83722 83726 83732 83740 211419
| 实验编号 | 温度 | 铝的规格 | 盐酸浓度 |
| ① | 20℃ | 铝片 | 5% |
| ② | 20℃ | 铝片 | 10% |
| ③ | 铝粉 | 10% | |
| ④ | 30℃ | 铝片 | 5% |
(2)用②和③来探究铝的状态对反应速率的影响,小林进行实验③时的温度为 ;
(3)要探究温度对反应速率的影响,小林设计的实验组合是 (填写实验编号);
(4)小林设计实验组合①②的目的是 ;
(5)实验探究时,小林每次收集的氢气均为30mL,则实验中他还应记录的实验数据是 ;
(6)在进行上述铝与稀盐酸反应时,粗心的小林不小心将氢氧化钠溶液倒入了铝片中,发现也有气泡产生,好奇的他继续进行了如下实验探究:
【提出问题】铝与氢氧化钠溶液反应时生成的气体是什么?
【进行猜想】猜想①:可能是CO2;猜想②:可能是O2;猜想③:可能是H2.
你认为猜想 是不合理的,理由是 ;
【实验方案】①收集气体:实验时气体收集的方法是 ;
②检验气体:验证猜想②的方法是 ;
【得出结论】铝与氢氧化钠溶液反应的方程式为:
2Al+2NaOH+2H2O=2 +3H2↑(在横线上填上化学式).