石灰石是我省的主要矿产之一.学校研究性学小组为了测定当地矿山石灰石中碳酸钙的质量分数.取来了矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
(1)哪几次反应中矿石有剩余?
(2)试计算这种石灰石中碳酸钙的质量分数.
(3)上表中m值是______.
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2 的质量/g | 1.76 | 3.52 | 4.4 | m |
(2)试计算这种石灰石中碳酸钙的质量分数.
(3)上表中m值是______.
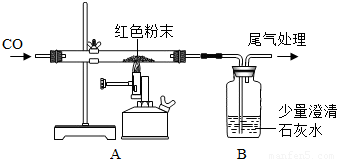
红色粉末是由Cu、Fe2O3二种固体组成,某同学为测定其成分做了如下实验:称取该粉末5.0g装入硬质玻璃管中,
(1)请用Ⅰ组实验数据计算红色粉末中Fe2O3的质量分数.
(2)不选择Ⅱ组实验数据的原因是______.
0 83327 83335 83341 83345 83351 83353 83357 83363 83365 83371 83377 83381 83383 83387 83393 83395 83401 83405 83407 83411 83413 83417 83419 83421 83422 83423 83425 83426 83427 83429 83431 83435 83437 83441 83443 83447 83453 83455 83461 83465 83467 83471 83477 83483 83485 83491 83495 83497 83503 83507 83513 83521 211419
| 反应前 | 反应后 | |
| Ⅰ组 | 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ组 | 洗气瓶和所盛溶液的总质量为180.0g | 洗气瓶和瓶中物质的总质量为183.1g |
(2)不选择Ⅱ组实验数据的原因是______.

 一氧化碳
一氧化碳 一氧化碳
一氧化碳
