海洋是个巨大的宝库,为人类提供了宝贵的自然资源.
(1)食用海鱼摄取的主要营养素是 .
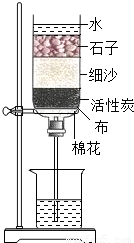
(2)如图1为海水淡化装置,利用的能源是 ,获得的蒸馏水属于 .
A.单质 B.化合物 C.混合物
(3)利用海水可制取许多化工产品.用海水制食盐,常通过海水晒盐得到粗盐,粗盐中含有少量的CaCl2、Na2SO4等杂质.除去上述杂质,先加过量的BaCl2溶液除去,再加过量 溶液除去CaCl2和过量的BaCl2,生成的沉淀经 除去,最后加入 调节pH,蒸发、结晶,制得粗盐.
(4)用氯化钠和碳酸氢铵可制备碳酸氢钠和氯化铵,该反应化学方程式可表示为;NaCl+NH4HCO3=NaHCO3+NH4Cl.20℃时,按上述化学方程式中反应物的质量比,向100克水中加入11.7克NaCl和15.8克NH4HCO3,理论上从溶液中提出晶体的质量为 g.
资料:20℃时四种物质的溶解度如下:假设它们同时溶解在水中各自的溶解度不变,
(5)从海水中提取溴常用吹出法,即用氯气将海水里的溴化钠中的溴置换出来,再用空气或水蒸气吹出溴.流程示意图如图2:
①写出氯气置换出溴单质的化学方程式; ;该反应在pH=3的酸性条件下进行,可用 测定反应液的酸碱度.
②吹出的溴和大量空气混合在一起进入吸收塔(吸收塔中发生的反应;Br2+SO2+2H2O?H2SO4+2HBr).根据流程图分析,通入SO2的目的是 .

(1)食用海鱼摄取的主要营养素是 .
(2)如图1为海水淡化装置,利用的能源是 ,获得的蒸馏水属于 .
A.单质 B.化合物 C.混合物
(3)利用海水可制取许多化工产品.用海水制食盐,常通过海水晒盐得到粗盐,粗盐中含有少量的CaCl2、Na2SO4等杂质.除去上述杂质,先加过量的BaCl2溶液除去,再加过量 溶液除去CaCl2和过量的BaCl2,生成的沉淀经 除去,最后加入 调节pH,蒸发、结晶,制得粗盐.
(4)用氯化钠和碳酸氢铵可制备碳酸氢钠和氯化铵,该反应化学方程式可表示为;NaCl+NH4HCO3=NaHCO3+NH4Cl.20℃时,按上述化学方程式中反应物的质量比,向100克水中加入11.7克NaCl和15.8克NH4HCO3,理论上从溶液中提出晶体的质量为 g.
资料:20℃时四种物质的溶解度如下:假设它们同时溶解在水中各自的溶解度不变,
| 物质 | NaCl | NH4CO3 | NH4Cl | NaHCO3 |
| 溶解度 | 36.0 | 21.6 | 37.2 | 9.6 |
①写出氯气置换出溴单质的化学方程式; ;该反应在pH=3的酸性条件下进行,可用 测定反应液的酸碱度.
②吹出的溴和大量空气混合在一起进入吸收塔(吸收塔中发生的反应;Br2+SO2+2H2O?H2SO4+2HBr).根据流程图分析,通入SO2的目的是 .

牙膏是生活中常见的物质,其配料成份有摩擦剂、增白剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校兴趣小组想研究牙膏摩擦剂的成分.
【提出问题1】某品牌牙膏中是否含有碳酸钙?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
①取少量牙膏于试管中,加入过量稀盐酸,出现气泡,将气体通入澄清石灰水中,石灰水变浑浊,证明摩擦剂中含有______离子;
②取实验①中的溶液,加入草酸铵溶液,生成白色沉淀-草酸钙,请写出该反应的化学方程式______.
【提出问题2】该牙膏中碳酸钙的含量是多少?
【实验步骤】
(1)按图连接好装置后,发现一处明显的错误,改正为______;

(2)重新连接好装置,并______;
(3)在B装置中加入牙膏样品8.00克;
(4)______K1,______K2(填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至______,停止滴加盐酸;
(5)______,至C中不再产生沉淀;
(6)将C装置中的固体混合物过滤、______、烘干后称量其质量;
(7)重复实验.
(已知此品牌牙膏中的摩擦剂为碳酸钙,且其他成分不和盐酸反应,装置内试剂均足量.)
【实验数据】重复实验,3次数据记录如下:
【实验分析及数据处理】
(1)上述数据能否由托盘天平测得?______.
(2)若没有A装置,则测定结果将______. (填“偏大”、“偏小”或“不变”)
(3)D装置的作用是______.
(4)据上表数据,计算该牙膏样品中碳酸钙的含量是多少?
写出计算过程.
【实验反思】
(1)重复实验,取平均值的意义在于______.
(2)下列各项措施中,能提高测定准确度的是______(填序号)
a.在装置A、B之间增加盛有浓硫酸的洗气瓶
b.在装置B、C之间增加盛有饱和碳酸氢钠的洗气瓶
c.缓缓滴加稀盐酸.
0 81621 81629 81635 81639 81645 81647 81651 81657 81659 81665 81671 81675 81677 81681 81687 81689 81695 81699 81701 81705 81707 81711 81713 81715 81716 81717 81719 81720 81721 81723 81725 81729 81731 81735 81737 81741 81747 81749 81755 81759 81761 81765 81771 81777 81779 81785 81789 81791 81797 81801 81807 81815 211419
【提出问题1】某品牌牙膏中是否含有碳酸钙?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
①取少量牙膏于试管中,加入过量稀盐酸,出现气泡,将气体通入澄清石灰水中,石灰水变浑浊,证明摩擦剂中含有______离子;
②取实验①中的溶液,加入草酸铵溶液,生成白色沉淀-草酸钙,请写出该反应的化学方程式______.
【提出问题2】该牙膏中碳酸钙的含量是多少?
【实验步骤】
(1)按图连接好装置后,发现一处明显的错误,改正为______;

(2)重新连接好装置,并______;
(3)在B装置中加入牙膏样品8.00克;
(4)______K1,______K2(填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至______,停止滴加盐酸;
(5)______,至C中不再产生沉淀;
(6)将C装置中的固体混合物过滤、______、烘干后称量其质量;
(7)重复实验.
(已知此品牌牙膏中的摩擦剂为碳酸钙,且其他成分不和盐酸反应,装置内试剂均足量.)
【实验数据】重复实验,3次数据记录如下:
| 实验次数 | 实验1 | 实验2 | 实验3 |
| C装置中沉淀质量(g) | 3.93 | 3.94 | 3.95 |
(1)上述数据能否由托盘天平测得?______.
(2)若没有A装置,则测定结果将______. (填“偏大”、“偏小”或“不变”)
(3)D装置的作用是______.
(4)据上表数据,计算该牙膏样品中碳酸钙的含量是多少?
写出计算过程.
【实验反思】
(1)重复实验,取平均值的意义在于______.
(2)下列各项措施中,能提高测定准确度的是______(填序号)
a.在装置A、B之间增加盛有浓硫酸的洗气瓶
b.在装置B、C之间增加盛有饱和碳酸氢钠的洗气瓶
c.缓缓滴加稀盐酸.

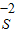 .
. 6H2O+ .
6H2O+ .