下列依据实验目的所设计的实验操作中,正确的是( )
A.A
B.B
C.C
D.D
| 选项 | 实验目的 | 实验操作 |
| A | 检验NaCl中含有Na2CO3 | 加水溶解 |
| B | 鉴别NaOH和Ca(OH)2溶液 | 加Na2CO3溶液 |
| C | 除去CaO中的CaCO3 | 加足量稀盐酸 |
| D | 除去CO2中的CO | 通入足量NaOH溶液 |
A.A
B.B
C.C
D.D
下表给出了化合物X和Y于两种温度下,在不同溶剂中的溶解度,某一样品中含60gX和10gY,采用降温结晶法提纯X时,得到 X晶体最多的溶剂是.( )
A.A
B.B
C.C
D.D
| 溶剂 | 10°C时的溶解度 | 80°C时的溶解度 | ||
| 化合物X | 化合物Y | 化合物X | 化合物Y | |
| A | 5 | 2 | 70 | 50 |
| B | 14 | 18 | 70 | 70 |
| C | 10 | 14 | 80 | 65 |
| D | 10 | 4 | 85 | 75 |
A.A
B.B
C.C
D.D
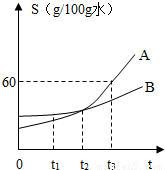
如图是A、B两种固体物质的溶解度曲线,依图回答:
① ℃时,A、B两物质的溶解度相等;
②t1℃时,10克水里最多能溶解3.5克B物质,则此温度下B物质的溶解度为 g/100g水;
③t3℃时,A物质饱和溶液的溶质的质量分数为 ;
④烧杯中盛有一定质量、温度为80℃、溶质为A的溶液,将其置于室温环境中,测定不同温度时析出固体A的质量.测定结果记录如下表.
不考虑水蒸发,则65℃时,该溶液是否为饱和溶液? (填“是”、“否”或“无法判断”).
0 81347 81355 81361 81365 81371 81373 81377 81383 81385 81391 81397 81401 81403 81407 81413 81415 81421 81425 81427 81431 81433 81437 81439 81441 81442 81443 81445 81446 81447 81449 81451 81455 81457 81461 81463 81467 81473 81475 81481 81485 81487 81491 81497 81503 81505 81511 81515 81517 81523 81527 81533 81541 211419
① ℃时,A、B两物质的溶解度相等;
②t1℃时,10克水里最多能溶解3.5克B物质,则此温度下B物质的溶解度为 g/100g水;
③t3℃时,A物质饱和溶液的溶质的质量分数为 ;
④烧杯中盛有一定质量、温度为80℃、溶质为A的溶液,将其置于室温环境中,测定不同温度时析出固体A的质量.测定结果记录如下表.
| 溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
| 析出固体A的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |

 Si+nCO↑.下列说法正确的是( )
Si+nCO↑.下列说法正确的是( )

 6H2O+ .
6H2O+ .