酸、碱溶液是化学常见的物质,依据所给内容回答问题:
下表是在不同温度下氢氧化钠的溶解度:
(1)氢氧化钠溶液中的溶质是 .20℃时,向100克水中加入100克氢氧化钠固体,所得溶液为 溶液(填“饱和”或“不饱和”),其溶液的质量是 克.
(2)在学习过程中,可以判断反应发生的方法有多种.
①向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应.
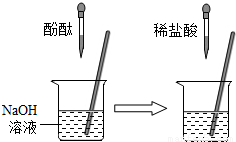
②在如图的实验中,当观察到的现象是 就可证明NaOH与HCl发生了反应.
③不使用指示剂或pH试纸等方法,也可证明反应发生.向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是 .
下表是在不同温度下氢氧化钠的溶解度:
| 温度/℃ | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | 31 | 91 | 111 | 129 | 313 | 336 |
(2)在学习过程中,可以判断反应发生的方法有多种.
①向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
②在如图的实验中,当观察到的现象是 就可证明NaOH与HCl发生了反应.
③不使用指示剂或pH试纸等方法,也可证明反应发生.向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是 .

某班学生分成两个小组,利用如图所示装置进行实验,请按要求回答问题:
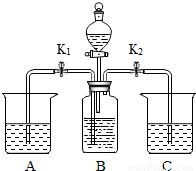
(1)第一小组同学的实验:
(2)第二小组同学的实验:

(1)第一小组同学的实验:
| 位置 | A | B | C | 分液漏斗 | |
| 药品 | 澄清石灰水 | 碳酸钠溶液 | 澄清石灰水 | 稀盐酸 | |
| 操作 | 关闭K1,打开K2和分液漏斗的活塞,缓慢滴加稀盐酸 | ||||
| 现象与结论 | 现象 | . | |||
| 有关化学方程式 | . | ||||
| 操作 | 关闭K2,打开K1 | ||||
| 现象 | B中液体沿导管流入A中,A中有白色沉淀产生 | ||||
| 该现象产生的原因 | . | ||||
| 位置 | A | B | C | 分液漏斗 |
| 药品 | 红色溶液 | 稀盐酸 | 紫色溶液 | 碳酸钠溶液 |
| 操作 | 关闭K1,打开K2和分液漏斗的活塞,缓慢滴加碳酸钠溶液 | |||
| 现象 | . | |||
| 操作 | 关闭K2,打开K1 | |||
| 现象 | B中液体沿导管流入A中,A中红色溶液变为无色 | |||
| A中的溶液 | . | |||
化学小组对金属钠产生了浓厚的兴趣,在老师的帮助下,提出了“金属钠能否置换出硫酸铜溶液中的铜?”“金属钠是否能在二氧化碳中燃烧?”等问题.请你参与他们的探究,并回答相应的问题:
查阅资料:①金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠.②金属钠还可以与水剧烈反应放出氢气.③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
实验探究:
实验1:探究金属钠是否能置换出硫酸铜溶液中的铜
实验2:探究金属钠是否能在二氧化碳中燃烧?
实验3:探究白色物质是什么?
实验反思:
(1)金属钠保存在煤油中的原因是 .
(2)实验3中③“向滤液中加入过量的氯化钙溶液”的原因是 .
查阅资料:①金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠.②金属钠还可以与水剧烈反应放出氢气.③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
实验探究:
实验1:探究金属钠是否能置换出硫酸铜溶液中的铜
| 实验操作 | 实验现象 | 结论与解释 |
| ①用镊子从煤油中取出一小块金属钠,用滤纸吸干表面煤油后投入硫酸铜溶液中 | 出现蓝色沉淀,但没有红色的物质析出 | 金属钠 (填“能”或“不能”)置换出硫酸铜溶液中的铜 |
| 同上,将金属钠投入水中,待反应结束后滴加酚酞溶液 | 溶液变红 | 钠与水反应的化学方程式是 . |
| 实验操作 | 实验现象 | 结论与解释 |
| 将燃烧的钠迅速伸入盛有CO2的集气瓶中 | 钠在CO2中继续燃烧,冷却,瓶内附着黑色颗粒,并粘附着白色物质. | 产物中一定有 . |
| 实验操作 | 实验现象 | 结论与解释 |
| ①取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液. | 溶液变成红色 | 产物中一定还有 |
| ②取该样品少量于试管里,滴加足量稀盐酸. | 有气泡冒出 | |
| ③取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的氯化钙溶液,出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液 | 无明显现象 |
(1)金属钠保存在煤油中的原因是 .
(2)实验3中③“向滤液中加入过量的氯化钙溶液”的原因是 .
某化验员取纯碱样品(含氯化钠)44g于烧杯中加水将其溶解,然后分几次逐滴加入溶质质量分数为20%的稀盐酸,并不断搅拌,称量,将得到的有关数据记录如下:(注:加盐酸时首先发生反应是:Na2CO3+HCl=NaHCO3+NaCl,然后是NaHCO3+HCl=NaCl+CO2↑+H2O)
(1)加入______g稀盐酸开始产生二氧化碳.
(2)计算恰好不再产生气体时,所得溶液的溶质质量分数.(保留一位小数)
0 81162 81170 81176 81180 81186 81188 81192 81198 81200 81206 81212 81216 81218 81222 81228 81230 81236 81240 81242 81246 81248 81252 81254 81256 81257 81258 81260 81261 81262 81264 81266 81270 81272 81276 81278 81282 81288 81290 81296 81300 81302 81306 81312 81318 81320 81326 81330 81332 81338 81342 81348 81356 211419
| 加入稀盐酸质量/g | 73 | 74 | 146 | 147 | |
| 烧杯中溶液质量/g | 200 | 273 | 273.76 | 328.4 | 329.4 |
(2)计算恰好不再产生气体时,所得溶液的溶质质量分数.(保留一位小数)

