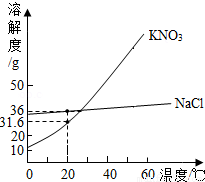
如图是KNO3和NaCl的溶解度曲线.据图回答:
(1)KNO3和NaCl两种饱和溶液的浓度相同时的温度是 ℃
(2)要从KNO3的溶液中析出晶体,通常采用的方法是 .
(3)在20℃时,某实验小组根据下表配制氯化钠溶液,计算并填写下表:
(4)若要得到溶质质量分数为20%以上的KNO3溶液,配制时的温度应不低于 ℃
(1)KNO3和NaCl两种饱和溶液的浓度相同时的温度是 ℃
(2)要从KNO3的溶液中析出晶体,通常采用的方法是 .
(3)在20℃时,某实验小组根据下表配制氯化钠溶液,计算并填写下表:
| 烧杯编号 | NaCl/g | H2O/g | 溶质的质量分数 |
| 1 | 10 | 90 | |
| 2 | 30 | 70 |

铁、铝、铜是日常生活中使用最广泛的金属.
(1)上述三种金属中,人类最早大规模冶炼和使用的是
(2)常温下一些金属的物理性质数据如下:
分析上述数据,碎石用的大锤常用铁制而不用铝制,原因是 .
(3)金属铝与氧化铁在高温条件下能发生置换反应,其化学方程式为 .
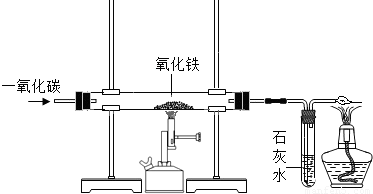
(4)炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可用如图所示装置进行实验:实验中玻璃管内的粉末由红色变为 色,该反应的化学方程式为 .
(1)上述三种金属中,人类最早大规模冶炼和使用的是
(2)常温下一些金属的物理性质数据如下:
| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
| 密度/ | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
| 熔点/℃ | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 2.5~3 | 2~2.9 | 2.5 | 4~5 | 1.5 |
(3)金属铝与氧化铁在高温条件下能发生置换反应,其化学方程式为 .
(4)炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可用如图所示装置进行实验:实验中玻璃管内的粉末由红色变为 色,该反应的化学方程式为 .

实验小组对铁的锈蚀按下表探究.室温时,将包有样品的滤纸包固定在橡胶塞上,迅速塞紧,装置如下图.观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如下表.
(1)实验①和②说明NaCl可以 (填“加快”或“减慢”)铁锈蚀的速率.
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是 (填“放热”或“吸热”)过程.
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是 .
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成.

| 序号 | 样品 | 量筒起始读数 /mL | 量筒最终读数 /mL | 所需时间 /min |
| ① | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
| ② | l g铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
| ③ |
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是 (填“放热”或“吸热”)过程.
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是 .
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成.

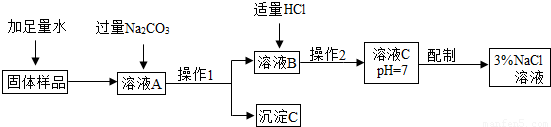
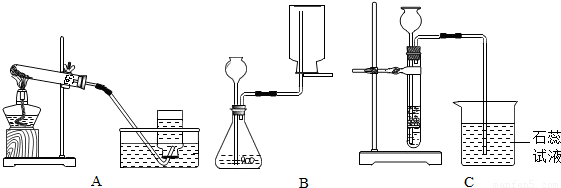
三瓶没有标签的白色粉末是Ba(NO3)2、MgCl2和CaO.请设计一个实验方案进行鉴别,并贴上标签.叙述实验操作、预期现象和结论.
提供的试剂有:蒸馏水 提供的仪器有:试管,胶头滴管
0 80821 80829 80835 80839 80845 80847 80851 80857 80859 80865 80871 80875 80877 80881 80887 80889 80895 80899 80901 80905 80907 80911 80913 80915 80916 80917 80919 80920 80921 80923 80925 80929 80931 80935 80937 80941 80947 80949 80955 80959 80961 80965 80971 80977 80979 80985 80989 80991 80997 81001 81007 81015 211419
提供的试剂有:蒸馏水 提供的仪器有:试管,胶头滴管
| 实验操作 | 预期现象与结论 |