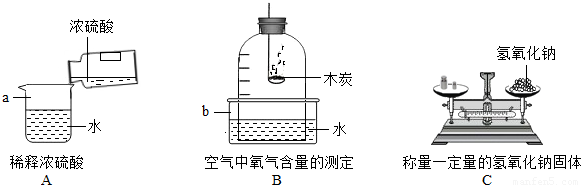
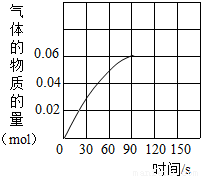
氢氧化钠与盐酸发生中和反应的化学方程式为 .
(1)为证明中和反应是放热反应,某小组进行了如如图所示的实验操作:根据如图实验,甲同学认为:NaOH与稀盐酸发生的中和反应是放热反应.乙同学认为:甲同学得出这个结论的依据不科学,理由是 .

(2)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、D、E的五只烧杯中各装入36.5g 溶质质量分数为5%、10%、15%、20%、25%的盐酸,再向上述五只烧杯中分别加入40g20% 的氢氧化钠溶液,最后测量其温度,数据记录如下:
【实验结论】影响中和反应放出热量多少的因素是 .
【交流反思】反应后,烧杯内溶液pH最小的是 (2分,填烧杯编号).
0 80248 80256 80262 80266 80272 80274 80278 80284 80286 80292 80298 80302 80304 80308 80314 80316 80322 80326 80328 80332 80334 80338 80340 80342 80343 80344 80346 80347 80348 80350 80352 80356 80358 80362 80364 80368 80374 80376 80382 80386 80388 80392 80398 80404 80406 80412 80416 80418 80424 80428 80434 80442 211419
(1)为证明中和反应是放热反应,某小组进行了如如图所示的实验操作:根据如图实验,甲同学认为:NaOH与稀盐酸发生的中和反应是放热反应.乙同学认为:甲同学得出这个结论的依据不科学,理由是 .

(2)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、D、E的五只烧杯中各装入36.5g 溶质质量分数为5%、10%、15%、20%、25%的盐酸,再向上述五只烧杯中分别加入40g20% 的氢氧化钠溶液,最后测量其温度,数据记录如下:
| 烧杯编号 | A | B | C | D | E |
| 盐酸的溶质质量分数 | 5% | 10% | 15% | 20% | 25% |
| 反应后溶液温度(℃) | 24℃ | 34℃ | 46℃ | 54℃ | 54℃ |
【交流反思】反应后,烧杯内溶液pH最小的是 (2分,填烧杯编号).