在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案设计、实施和评价.
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(常温下)他们先测定出某NaOH溶液的pH 7(填“大于”、“等于”或“小于”),然后将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后再测定其pH,发现其pH小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且 过量.
(2)方案二:利用酸碱指示剂
①探究稀H2SO4与NaOH溶液的反应
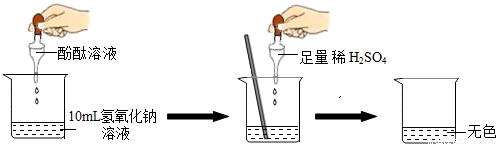
如图所示进行实验.当滴入几滴酚酞溶液后,溶液由无色变为 色.根据上述过程中的颜色变化,确定稀H2SO4与NaOH溶液发生了反应,该反应的化学方程式为 .
②探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量
根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2溶液与、紫色石蕊溶液、Na2CO3粉末设计实验方案,请你判断并分析:
方案三中反应的化学方程式为 .上述设计的实验方案中,不正确的是 (填“方案一”、“方案二”或“方案三”).错误的原因是 .请你再设计一个实验方案确定稀H2SO4是否过量,你选用 (填药品或者方法).
0 79553 79561 79567 79571 79577 79579 79583 79589 79591 79597 79603 79607 79609 79613 79619 79621 79627 79631 79633 79637 79639 79643 79645 79647 79648 79649 79651 79652 79653 79655 79657 79661 79663 79667 79669 79673 79679 79681 79687 79691 79693 79697 79703 79709 79711 79717 79721 79723 79729 79733 79739 79747 211419
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(常温下)他们先测定出某NaOH溶液的pH 7(填“大于”、“等于”或“小于”),然后将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后再测定其pH,发现其pH小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且 过量.
(2)方案二:利用酸碱指示剂
①探究稀H2SO4与NaOH溶液的反应

如图所示进行实验.当滴入几滴酚酞溶液后,溶液由无色变为 色.根据上述过程中的颜色变化,确定稀H2SO4与NaOH溶液发生了反应,该反应的化学方程式为 .
②探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量
根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2溶液与、紫色石蕊溶液、Na2CO3粉末设计实验方案,请你判断并分析:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的BaCl2溶液 | 出现白色沉淀 | 稀H2SO4过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀H2SO4过量 |
| 方案三 | 取样,加入Na2CO3粉末 | 有气体产生 | 稀H2SO4过量 |

 4Al2O3+9Fe,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作.回答下列问题:
4Al2O3+9Fe,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作.回答下列问题: