小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的.他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验一 | 实验二 | 实验三 | |
实验 方案 |  | 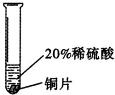 |  |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | ________ | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | ________ |
| 三种金属在金属活动性顺序中的相对位置关系是________(填①②③) | |||
(2)实验一所发生反应的化学方程式是________.
(3)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是________.(填化学式)
【归纳】比较金属活动性强弱的方法有:通过金属与酸溶液反应判断金属活动性强弱;还有________.
 课外小组研究“影响H2O2 生成O2反应速率的因素”的课题.通过查阅资料,他们提出如下猜想.
课外小组研究“影响H2O2 生成O2反应速率的因素”的课题.通过查阅资料,他们提出如下猜想.
【提出猜想】催化剂和反应物浓度都会影响H2O2 生成O2的反应速率
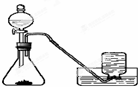
【实验过程】实验装置如图:
实验操作:检查装置的气密性良好.将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.
实验记录:
| 实验编号 | ① | ② | ③ |
| 反应物 | 5%H2O250mL | 5%H2O2________ | 3%H2O250mL |
| 加入固体 | 0.5gCuO | 0.5gMnO2 | 0.5gMnO2 |
| 收集等体积O2所需时间 | 105s | 45s | 78s |
(2)充分反应后,将实验②中剩余物质里的MnO2提取的方法是________;
【结论】该探究过程得出的结论是________;
【反思】H2O2在常温加入MnO2后反应速率加快.小敏提出,为了更好的证明二氧化锰是否对H2O2 生成O2的反应速率有影响,还应该增加一组对比实验.该实验选用的药品和用量为________;
【实验拓展】小敏用收集的气体进行氧气的性质实验.
(1)铁丝在氧气中燃烧,其反应的化学方程式为________;
(2)小敏发现用收集的气体进行铁丝燃烧实验时,没有产生明显的火星四射现象.造成这种结果的可能原因是________.
 符合图装置设计意图的有
符合图装置设计意图的有