某化学兴趣小组对一包干燥的红色粉末组成进行探究.请你参与并回答有关问题.
【教师提醒】它由Cu、Fe2O3二种固体中的一种或两种组成.
【提出猜想】红色粉末可能的组成有:①只有Cu;②只有______;③是Cu、Fe2O3的混合物
【资料获悉】Cu在FeCl3溶液中发生反应:2FeCl3+Cu═2FeCl2+CuCl2
【实验探究】
(1)甲同学取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解.甲同学认为可以排除猜想中的①和③,而乙同学认为只能排除猜想①,你认为______的观点正确(填“甲”或“乙”).
 (2)丙同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右图在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
(2)丙同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右图在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
【交流讨论】
(1)在装置A中先通CO气体的作用是______.
(2)应该选择______组的实验数据计算来确定红色粉末的组成.最终计算结果表明:该红色粉末的组成是猜想中的第______组(填序号).
(3)写出A装置中发生反应的化学方程式______ 2Fe+3CO2
0 68247 68255 68261 68265 68271 68273 68277 68283 68285 68291 68297 68301 68303 68307 68313 68315 68321 68325 68327 68331 68333 68337 68339 68341 68342 68343 68345 68346 68347 68349 68351 68355 68357 68361 68363 68367 68373 68375 68381 68385 68387 68391 68397 68403 68405 68411 68415 68417 68423 68427 68433 68441 211419
【教师提醒】它由Cu、Fe2O3二种固体中的一种或两种组成.
【提出猜想】红色粉末可能的组成有:①只有Cu;②只有______;③是Cu、Fe2O3的混合物
【资料获悉】Cu在FeCl3溶液中发生反应:2FeCl3+Cu═2FeCl2+CuCl2
【实验探究】
(1)甲同学取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解.甲同学认为可以排除猜想中的①和③,而乙同学认为只能排除猜想①,你认为______的观点正确(填“甲”或“乙”).
 (2)丙同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右图在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
(2)丙同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右图在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:| 反应前 | 反应后 | |
| Ⅰ组 | 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ组 | 洗气瓶和所盛溶液的总质量为180.0g | 洗气瓶和瓶中物质的总质量为183.1g |
(1)在装置A中先通CO气体的作用是______.
(2)应该选择______组的实验数据计算来确定红色粉末的组成.最终计算结果表明:该红色粉末的组成是猜想中的第______组(填序号).
(3)写出A装置中发生反应的化学方程式______ 2Fe+3CO2
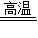 4Fe+CO2↑,某同学设计了一个实验,证明氧化铁中含有氧元素,并测定氧化铁中氧元素的质量分数,实验装置如图.
4Fe+CO2↑,某同学设计了一个实验,证明氧化铁中含有氧元素,并测定氧化铁中氧元素的质量分数,实验装置如图.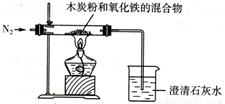

 xFe+yH2O Fe3C+2H2
xFe+yH2O Fe3C+2H2 3Fe+CH4
3Fe+CH4 3CO2+6H2O+8Fe
3CO2+6H2O+8Fe







