甲、乙两个研究性学习小组分别制备氨气,并利用氨气的性质(氨气与灼热的氧化铜反应,生成铜、水和氮气)来验证分子中氮、氢原子个数比,设计了如下实验流程:

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.
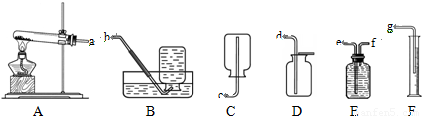
下图A、B、C为甲、乙两小组制备氨气时可能用到的装置,D为盛有足量浓硫酸的洗气瓶.

甲小组测得:反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g;生成的氮气在标准状况下的体积V1L(已知标准状况下,22.4L氮气的质量是28g).
乙小组测得:洗气前装置D的质量m3g、洗气后装置后D的质量m4g;生成的氮气在标准状况下的体积V2L.
请回答下列问题:
(1)写出仪器a的名称:
(2)检查A装置气密性的具体操作方法是 .
(3)甲、乙两小组选择了不同方法制备氨气,请将实验装置的字母编号和制备原理填写在下表空格中.
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为 .
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比小于理论值,其原因是 . 为此,乙小组在原有实验流程的基础上,在 的位置增加了一个装有足量药品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,也得出了合理的实验结果.该药品的名称是 .
0 63893 63901 63907 63911 63917 63919 63923 63929 63931 63937 63943 63947 63949 63953 63959 63961 63967 63971 63973 63977 63979 63983 63985 63987 63988 63989 63991 63992 63993 63995 63997 64001 64003 64007 64009 64013 64019 64021 64027 64031 64033 64037 64043 64049 64051 64057 64061 64063 64069 64073 64079 64087 211419

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.
下图A、B、C为甲、乙两小组制备氨气时可能用到的装置,D为盛有足量浓硫酸的洗气瓶.

甲小组测得:反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g;生成的氮气在标准状况下的体积V1L(已知标准状况下,22.4L氮气的质量是28g).
乙小组测得:洗气前装置D的质量m3g、洗气后装置后D的质量m4g;生成的氮气在标准状况下的体积V2L.
请回答下列问题:
(1)写出仪器a的名称:
(2)检查A装置气密性的具体操作方法是 .
(3)甲、乙两小组选择了不同方法制备氨气,请将实验装置的字母编号和制备原理填写在下表空格中.
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为 ① |
| 乙小组 | ② | 浓氨水、氢氧化钠 |
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比小于理论值,其原因是 . 为此,乙小组在原有实验流程的基础上,在 的位置增加了一个装有足量药品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,也得出了合理的实验结果.该药品的名称是 .