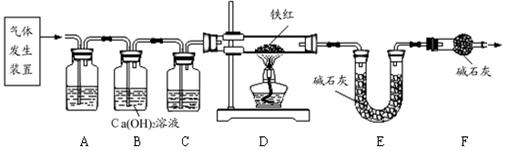
某校化学研究小组对某铜器表面的绿色铜锈展开探究,请回答有关问题。
【实验过程】
(1)动手实验
实验一:
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量铜锈于试管中,加入适量稀硫酸 | 固体溶解,产生气泡,溶液呈蓝色 | 铜锈溶解后形成的溶液中含有的阳离子是 ※ (写化学符号) |
| b.将生成气体通入澄清石灰水 | | 铜锈中含有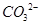 |
【实验结论】综合以上两个实验,可以确认铜锈中含有 种元素。
(2)探究铜生锈的条件
【猜想】同学们对空气中有哪些物质参与了铜的生锈作出以下三种猜想:
①CO2、H2O ②O2、H2O ③CO2、H2O、O2
根据铜锈组成元素并结合铁生锈的知识,你认为上述猜想错误的是 (填序号)。
【实验设计】为验证另外两种猜想,同学们设计了下图中A、B两个对比实验,请你在方框内完成实验B的设计(语言叙述或画图说明均可)。

【预计结论】若A中的铜生锈,B中的铜不生锈,则正确的猜想是 (填序号)。
在金属活动性顺序里,钠位于铜之前。某化学兴趣小组发现,将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,却未置换出红色的铜。该小组同学对此现象进行了如下探究:
【查阅资料】钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应。
【分析与讨论】
(1)在实验室中通常将钠保存在煤油里,煤油的作用是 。
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低。对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为 同学的猜想不合理,请从化合价的角度解释原因: 。
【进行实验】该小组同学通过实验验证钠与水反应的产物,装置如下图: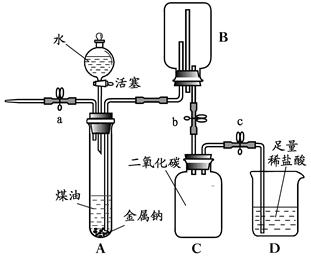
注:煤油的密度为0.8g/mL,与水不互溶。
| | 实验操作 | 实验现象及分析 |
| ① | 打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞。 | 实验现象为:液体分层,钠熔成银白色小球,在液体分层的界面上跳动,产生大量气泡,下层液体逐渐被压入B中。 钠的物理性质有: (任写两条)。 |
| ② | 打开止水夹b,待B中部分液体进入C中,迅速关闭止水夹b。 | 发生反应的化学方程式为: 。 |
| ③ | 打开止水夹c。 | 实验现象为:D中液体 ,C中产生气泡。 |
| ④ | 打开止水夹a,通过分液漏斗向大试管中逐滴加水,将燃着的木条伸至装置左端尖嘴导管口。 | 实验现象为:气体燃烧,产生 色火焰。 |
| ⑤ | 在火焰上方罩一个干冷的烧杯。 | 实验现象为:烧杯内壁出现 。 |
一次,小刚在实验室看到了右图情景:
他首先想到药品可能变质了,那么NaOH溶液在空气中变质的化学方程式为______________________________________;
小刚利用实验室的三种试剂(氯化钙溶液、稀盐酸、酚酞试剂)对这瓶“NaOH溶液”展开了探究。
[提出猜想]
猜想①:氢氧化钠溶液没有变质
猜想②:____________________
猜想③:氢氧化钠溶液完全变质
[实验探究]
| 方 案 | 现 象 | 结 论 | |
| I | 取少量溶液于试管中,滴入足量__________试剂 | 产生大量气泡 | 猜想①不成立 |
| II | 取少量溶液于试管中,滴加酚酞试剂 | 溶液变红 | 溶液中一定含NaOH |
| III | a.取少量溶液于试管中,滴加足量________试剂; | ____________ | 猜想②成立 |
| b.向a中所得溶液中滴加酚酞 | 溶液变红 | ||
[反思评价]氢氧化钠溶液暴露在空气中容易变质,故应____________保存。

 x Fe + y H2O,Fe3C + 2 H2
x Fe + y H2O,Fe3C + 2 H2 3 Fe + CH4。
3 Fe + CH4。
 3 CO2 + 6H2O + 8 Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
3 CO2 + 6H2O + 8 Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。