��Ŀ����
̽����������ԭ������һ����Ҫ�Ļ���ԭ�ϣ�ij��ȤС�������������о���
�������Ʊ��������̷��Ʊ�����ԭ���۵Ĺ����������£�
�ֻ�ԭ�����л��������������������Fe3C���ʣ����������ڸ����½�һ����ԭ���䷴Ӧ����ʽΪFexOy + y H2 x Fe + y H2O��Fe3C + 2 H2
x Fe + y H2O��Fe3C + 2 H2 3 Fe + CH4��
3 Fe + CH4��
��1��д����������������CO��Ӧ�Ļ�ѧ����ʽ�� ��
��2�������мӽ�̿�����ó��˿�������CO�⣬���� ��
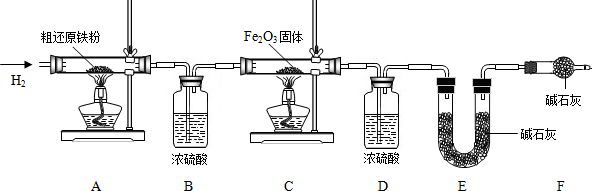
�������ⶨ��Ϊ�õ�����ԭ���۲��ⶨ�ֻ�ԭ����������̼Ԫ�ص�����������������װ�ý���ʵ�顣��֪3 CH4 + 4 Fe2O3 3 CO2 + 6H2O + 8 Fe������ÿ����Ӧ����ȫ���Ҳ�����װ����ԭ�п����Բⶨ�����Ӱ�죩��
3 CO2 + 6H2O + 8 Fe������ÿ����Ӧ����ȫ���Ҳ�����װ����ԭ�п����Բⶨ�����Ӱ�죩��
��3����Ҫʵ�鲽�����£�
�ٰ�˳����װ���������װ�õ������ԣ�������Ʒ�ͱ�Ҫװ�õ��������ڵ�ȼA���ƾ��ƣ��ۻ���ͨ�봿�������H2���ܵ�ȼC���ƾ��ƣ��ݷֱ�Ϩ��A����C���ƾ��ƣ����ٻ���ͨ������H2�����ٴγ�����Ҫװ�õ�������
�������Ⱥ�˳���Ǣ١��ۡ� ���ݡ��ޡ���(����ĸ)
A���ڡ��� B���ܡ���
��4������۵�Ŀ���� ����֤�ò���Ŀ�Ĵﵽ��ʵ�鷽���� ��
��5����ȱ��װ��D����������Ԫ�ص����������� (�ƫ����ƫС"����")��
��6���ֻ�ԭ������Ʒ������Ϊ20.000 g��װ��B��E�ֱ�����0.360 g��0.440 g���������Ʒ����̼Ԫ�ص����������� ����Ԫ�ص����������� ��
̽������1�� ��2���ṩ���� ��3��B
��2���ṩ���� ��3��B
��4����ȥװ���ڵ������������������ֹ������ը
�ռ�β����ȼ��������
��5������
��6��0��6% 1.6%
�������������̽��һ��1��һ����̼�����»�ԭ�����������������Ͷ�����̼�� ����2��̿���������������ã�һ���Dz���һ����̼����һ���Dz������£���3��˳��Ϊ��˳����װ���������װ�õ������ԣ�������Ʒ�ͱ�Ҫװ�õ�����������ͨ�봿�������H2����ȼC���ƾ��ƣ���ȼA���ƾ��ƣ��ֱ�Ϩ��A����C���ƾ��ƣ��ٻ���ͨ������H2���ٴγ�����Ҫװ�õ���������4������۵�Ŀ�����ž�װ���еĿ�������ֹ������ը�������ռ�β����ȼ��֤���ȣ���5��Ũ��������������ˮ����������ʯ��Ҳ��������ˮ������������ȱ��װ��D����������Ԫ�ص��������������䣻��6�������ɼ�������Ϊ
����2��̿���������������ã�һ���Dz���һ����̼����һ���Dz������£���3��˳��Ϊ��˳����װ���������װ�õ������ԣ�������Ʒ�ͱ�Ҫװ�õ�����������ͨ�봿�������H2����ȼC���ƾ��ƣ���ȼA���ƾ��ƣ��ֱ�Ϩ��A����C���ƾ��ƣ��ٻ���ͨ������H2���ٴγ�����Ҫװ�õ���������4������۵�Ŀ�����ž�װ���еĿ�������ֹ������ը�������ռ�β����ȼ��֤���ȣ���5��Ũ��������������ˮ����������ʯ��Ҳ��������ˮ������������ȱ��װ��D����������Ԫ�ص��������������䣻��6�������ɼ�������Ϊ

48 132 0.440g
0.440g �����
�����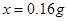
���� ����Ϊ0.16g����
����Ϊ0.16g���� ����Ϊ
����Ϊ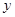
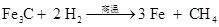
180 16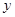 0.16g
0.16g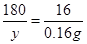 �����
�����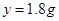
 �е�����Ϊ
�е�����Ϊ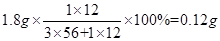
����Ʒ��̼Ԫ�ص���������Ϊ
����Ʒ����̼Ԫ�ص�����������6%��ͬ����Ԫ�ص�����������1.6%��
���㣺̽������ijɷ�
����������һ���dz����͵�̽���⣬��Ŀ����֪ʶ��û��ѧ������Ϊİ���������ص㿼��ķ�Ӧ��˼�룬װ�õȣ�����������Ŀ��Ҫ���£���ϸ���⼴�ɡ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�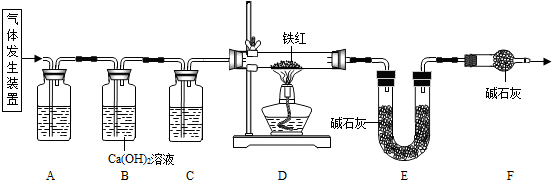


 x Fe + y H2O��Fe3C
+ 2 H2
x Fe + y H2O��Fe3C
+ 2 H2 3 Fe + CH4��
3 Fe + CH4��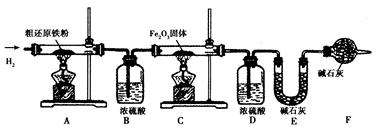
 3 CO2 + 6H2O + 8 Fe������ÿ����Ӧ����ȫ���Ҳ�����װ����ԭ�п����Բⶨ�����Ӱ�죩��
3 CO2 + 6H2O + 8 Fe������ÿ����Ӧ����ȫ���Ҳ�����װ����ԭ�п����Բⶨ�����Ӱ�죩��

 x Fe+y H2O��Fe3C+2H2
x Fe+y H2O��Fe3C+2H2


 x Fe + y H2O��Fe3C + 2H2
x Fe + y H2O��Fe3C + 2H2 3 Fe + CH4��
3 Fe + CH4��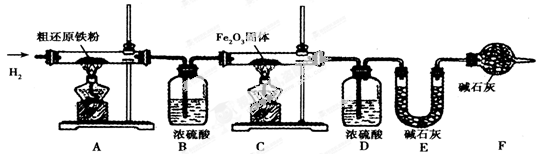
 3 CO2 + 6H2O + 8 Fe������ÿ����Ӧ����ȫ���Ҳ�����װ����ԭ�п����Բⶨ�����Ӱ�죩��
3 CO2 + 6H2O + 8 Fe������ÿ����Ӧ����ȫ���Ҳ�����װ����ԭ�п����Բⶨ�����Ӱ�죩��