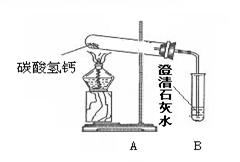
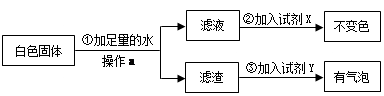
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如下图所示的实验。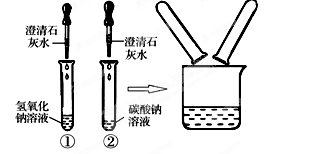
⑴写出试管②中碳酸钠与氢氧化钙反应的化学方程式:[来源:学#科#网]
▲ 。
⑵实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究。
【提出问题】滤液中除水外还含有哪些物质?
【猜想】 小红认为:只含氢氧化钠;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是 ▲ (写一种猜想)。
【实验设计】设计一个简单的实验证明你的猜想正确。
| 实验步骤 | 实验现象 | 实验结论 |
| 取样品于试管中, ▲ __. | _________▲__________ | 你的猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | 自己的猜想不成立 |
▲ 。
(3分)通过学习化学,我们知道氧气能使带火星的木条复燃,那么能使带火星的木条复燃的是否一定是纯氧呢?为了弄清这个问题,才仕实验学校化学小组进行了如下探究:
①取5个大小相同的集气瓶,分别编为1、2、3、4、5号,并分别使瓶内留有占集气瓶容积10%、20%、30%、40%、50%的水(余下为空气),用玻璃片盖住并倒扣在装有水的水槽中。
②分别用排水法向上述5个瓶子中通入氧气,小心地把5个瓶内的水排完后,用玻璃片盖住瓶口,取出正放好。
③将带火星的木条伸入5个瓶中,观察到的现象如下:
| 编号 | 1 | 2 | 3 | 4 | 5 |
| 现象 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
(1)从观察到的现象可知,使带火星的木条复燃所需氧气的最小体积分数介于 号瓶与 号瓶之间。
(2)用排水法收集满氧气后,4号瓶中氧气的体积分数约为 ;
(提示:空气中氧气的体积分数约为21%)
(3)若要得到更准确的体积分数范围,只要调整①步骤中集气瓶内水的体积,并重复上述实验即可,你认为调整后瓶内水占集气瓶容积的体积分数为 。
(7分)竹子是“有节、中空、四季常绿”的植物。同学们对竹子中的气体成分展开了探究,测定其成分。
(1)收集竹子中的气体。
小华提出:将一节竹子浸没在水中,在竹子上钻孔,用排水法收集气体。
小刚提出:可用注射器从竹子中抽取气体。
大家认为两人的想法都可行,于是分为A、B两组,在相同的条件下,A组采用小华的取气方法,B组采用小刚的取气方法,分别完成下面的实验。
(2)检验气体中是否含有二氧化碳气体。
| 实验步骤 | 实验现象 | 实验结论及化学方程式 |
| 向所取气体中加入 | | 气体中有二氧化碳。 |
【查阅资料】红磷的着火点为240 ℃,白磷的着火点为40 ℃。
【设计实验】同学们设计了如下图所示的方案一和方案二来测定氧气含量。

方案一 方案二
【进行实验】按上述两个方案进行多次实验。
【反思与评价】
a.实验中磷的量应为足量,原因是 。
b.两个方案的实验测定结果不同,测定结果比较准确的是方案 ,原因是 。
c.经过A、B两组同学的实验,A组测得的含氧量总是大于B组的,你认为原因是 。
火灾中含碳可燃物不完全燃烧产生的有害有毒的烟雾是造成人员死亡的杀手之一。化学兴趣小组的同学想研究烟雾的成分,他们利用实验室的设备模拟得到了火灾造成的烟雾,并进行处理后对所得的气体成分进行研究。
《提出猜想》(1)只有CO2;(2) (10) (3)既有CO2,也有CO。
《查阅资料》微量CO遇到浸有磷钼酸溶液的氯化钯黄色试纸,会立即变蓝;而CO2遇该试纸不变色
《设计方案》化学兴趣小组在老师的指导下,设计下图所示实验,通过观察装置B、装置C的实验现象,验证猜想。
《实验探究》完成下列实验报告。
| 实验步骤 | 实验现象 | 实验结论及化学方程式 |
| 挤压混合气体的储气罐,随即打开弹簧夹,通入混合气体。 观察装置B、装置C中的现象 | 装置B中的现象是: (11) 装置C中的现象是: (12) | 混合气体既有CO2,也有CO。 装置C中反应的化学方程式为: (13) |

(1)确认混合气体中存在CO、CO2实验结论的实验现象是 (14)
(2)写出装置D中发生反应的化学方程式 (15)
(3)装置A和C都是将气体通入澄清石灰水,但作用是不同的,请分别写出装置A和C中澄清石灰水的作用 (16) 、 (17)
(4)你认为第2套装置有哪些不合理之处: (18)
(5)上述2套装置都有一个共同的缺陷。请你提出改进方法,画出需添加的仪器,并作必要的文字说明 (19)
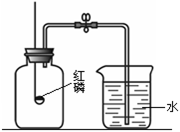
小华同学用右图所示装置进行中和反应实验,反应后为确定硫酸和氢氧化钠是否刚好完全反应,他取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论。
(1)写出该中和反应的化学方程式 (15) 。
(2)小亮认为小华的结论不准确,他认为除了“恰好中和”外还有“第二种可能性”,这种可能性是 (16) 。
(3)请你另外设计一个实验,验证述烧杯中的溶液是小亮推测的“第二种可能性”
| 实验操作 | 实验现象 | 实验结论 |
| 取样品, (17) | (18) | 确实是小亮推测的“第二种可能性” |
小林仔细阅读加碘自然盐包装袋上的说明(部分说明如图所示),提出问题与同学讨论并进行实验探究。
问题一:食盐加碘可以有效地预防
问题二:食盐是比较稳定的,而说明中强调“防热”是否因为受热会造成碘的损失?
《实验一》探究温度对碘损失率的影响
老师指导他们将一定浓度的碘酸钾溶液分成5等份,于不同温度下加热十分钟后,用硫代硫酸钠标准溶液测定碘酸钾浓度,计算碘损失率并记录如下:
| 温度 | 30℃水浴 | 50℃水浴 | 80℃水浴 | 100℃水浴 | 煮沸 |
| 碘损失率(%) | 0 | 0.3 | 0.67 | 1 | 5.56 |
实验后,小林建议妈妈烧菜时最好是菜出锅前再放碘盐。
问题三:烧菜时加醋对碘的损失率是否也有影响?
《实验二》探究酸碱性对碘损失率的影响
(1)此组对照实验,要控制在碘酸钾溶液的浓度和质量、加热的 和 均相同,溶液的 不同的条件下进行。
(2)实验中需要调节溶液的酸碱性,下列物质不能选用的是 (填序号)。
A.氢氧化钠 B.纯碱粉末 C.食盐晶体 D.食醋