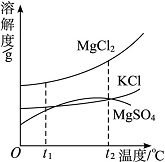
下列四个图像分别表示对应的四种操作过程,其中表示正确的图像是 ( )


|
|
|
|
 | |||||||
| |||||||
| |||||||
| |||||||
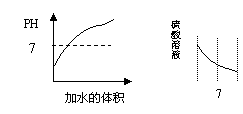
A.向pH=1的酸溶液中不断加水
B.向pH=1的硫酸溶液中逐滴加入pH=13的氢氧化钠溶液
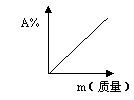
C.某温度下,向一定量的水中持续加入食盐并不断搅拌 (m表示加入食盐的质量,A%表示溶质质量分数)
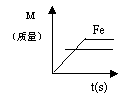
D.等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量M与反应时间t的关系图
为了测定某粉末状黄铜(铜锌合金)样品中铜的质量分数,洋洋同学取一定质量的黄铜样品放入烧杯中,再取40 g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 9.10 | 8.45 | 7.80 | 7.80 |
(1)上述反应的化学方程式为________________________;
(2)根据锌的质量列出求解第二次生成氢气质量(x)的比例式________________;
(3)所用稀盐酸中溶质的质量分数为________;
(4)用36.5%的浓盐酸配制40 g上述稀盐酸,需要浓盐酸的质量为________;
(5)黄铜样品中铜的质量分数为__________。
在日常生活中,我们发现切过咸菜的刀更容易生锈,而除锈用稀盐酸比稀硫酸快。为了进一步验证上述现象,某校师生做了以下相关分组实验,请你根据自己平时课堂学习的体验一起参与讨论并回答相关问题。
【步骤一】未打磨的铝片浸入氯化铜溶液中,迅速产生大量气泡和疏松的紫红色固体,并放热,片刻后溶液由蓝绿色变成无色。
(1)若要验证紫红色固体中是否含有氧化铜,可用________(填一试剂)加以检验。
【步骤二】未打磨的铝片浸入硫酸铜溶液中,一段时间内没有明显现象。
(2)比较步骤一、二,你能得出的结论是__________________________。
【步骤三】打磨过的铝片浸入硫酸铜溶液中,其操作、现象和结论见下表。
(3)试将下表“影响因素”选项前恰当的字母序号填入指定位置。
| 实验操作 | 实验现象 | 对比结论 |
| Ⅰ.一片用粗砂纸单向用力打磨3次,将其浸入硫酸铜溶液,片刻后用镊子取出。 | 现象一:粗砂纸打磨的在划痕处有少量气泡,附着少量疏松的紫红色固体。 现象二:粗砂纸打磨的片刻内现象不明显。 | 现象一与现象二对比,说明: ①____________ |
| Ⅱ.一片用特细砂纸往复打磨数次,再将其浸入硫酸铜溶液,片刻后取出。 | 现象三:特细砂纸打磨的表面产生较多细小气泡,表面均匀附着紫红色固体。 现象四:特细砂纸打磨的表面一段时间内没有明显现象。 | 现象三与现象一对比,说明:②________;现象四与现象三对比,说明:③__________ |
★影响因素:
A.打磨时用力程度及均匀程度不同 B.选用砂纸颗粒粗细程度不同
C.由于摩擦生热又形成了新的氧化膜
(4)比较步骤三各实验操作中用砂纸打磨的作用是______________________________。
(5)请仔细观察下图。
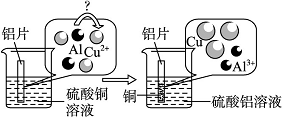
试从微观粒子变化的角度分析该反应的实质:_______________________________。
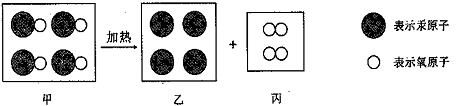
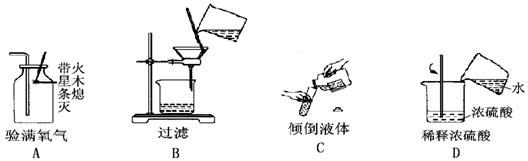 下列操作正确的是 ( )
下列操作正确的是 ( )
 0 g稀盐酸中,两者恰好完全反应。其化学方程式为Na2CO3+2HCl===2NaCl+H2O+CO2↑
0 g稀盐酸中,两者恰好完全反应。其化学方程式为Na2CO3+2HCl===2NaCl+H2O+CO2↑