题目内容
我国某地区有一种“冬天捞碱,夏天晒盐”的说法,这里的“碱”是指Na2CO3,“盐”是指NaCl。这样捞得的“碱”中含有少量NaCl。某化学课外活动小组为了解释捞碱、晒盐的原理和测定“碱”样品中Na2CO3的含量进行了以下探究。
[查阅资料]
Na2CO3和NaCl的溶解度曲线如图所示。
(1)根据图示回答:①t1 ℃时Na2CO3的溶解度为________ g;t2 ℃时Na2CO3的溶解度________(填“>”“=”或“<”)NaCl的溶解度。
②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度的降低而________(填“增大”“减小”或“不变”)。
③“夏天晒盐”是利用________(填字母)的方法,使NaCl晶体析出。

A.利用风吹日晒,使溶剂蒸发 B.升高温度,使NaCl的溶解度增大
[实验步骤]
第一步:称取34.6 g“碱”样品。
第二步:将该样品放入13 0 g稀盐酸中,两者恰好完全反应。其化学方程式为Na2CO3+2HCl===2NaCl+H2O+CO2↑
0 g稀盐酸中,两者恰好完全反应。其化学方程式为Na2CO3+2HCl===2NaCl+H2O+CO2↑
第三步:完全反应后,称得溶液的总质量为151.4 g,经计算可知释放出的二氧化碳的质量为13.2 g。
[数据分析]
(2)试计算:(结果保留一位小数)
①Na2CO3的相对分子质量。②34.6 g“碱”样品中碳酸钠的质量。③“碱”样品中Na2CO3的纯度。
[继续探究]
(3)计算反应后所得溶液中NaCl的质量分数。
答案:(1)①a = ②减小 ③A
(2)解:①23×2+12+3×16=106。
②设碳酸钠的质量为x,氯化钠的质量为y,
Na2CO3+2HCl===2NaCl+H2O+CO2↑
106 117 44
x y 13.2 g
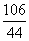 =
=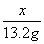 ,x=31.8 g;
,x=31.8 g;
 =
=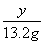 ,y=35.1 g。
,y=35.1 g。
③Na2CO3的纯度: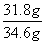 ×100%≈91.9%。
×100%≈91.9%。
答:①Na2CO3的相对分子质量为106;
②34.6 g“碱”样品中碳酸钠的质量为31.8 g;
③“碱”样品中Na2CO3的纯度为91.9%。
(3)解:氯化钠的总质量为:35.1 g+34.6 g-31.8 g=37.9 g,(37.9 g÷151.4 g)×100%≈25.0%。
答:反应后溶液中溶质的质量分数为25.0%。

 阅读快车系列答案
阅读快车系列答案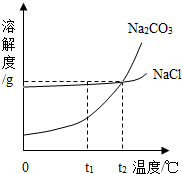 我国某地区有一种“冬天捞碱,夏天晒盐”的传统.这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中会含有少量NaCl.下图为Na2CO3和NaCl的溶解度曲线和部分温度下的溶解度表(单位是克),看图回答下列问题:
我国某地区有一种“冬天捞碱,夏天晒盐”的传统.这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中会含有少量NaCl.下图为Na2CO3和NaCl的溶解度曲线和部分温度下的溶解度表(单位是克),看图回答下列问题:(1)①t1℃时,NaCl的溶解度
②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度降低而
③“夏天晒盐”是利用
A.利用风吹日晒,使溶剂蒸发 B.升高温度,使NaCl溶解度增大
(2)根据下表分析:
| 温度 物质 |
0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2CO3 | 7.0 | 12.5 | 21.5 | 39.0 | 49.0 |
②下列几种说法中,正确的是
A.碳酸钠晶体的溶解度受温度影响较大
B.将含水各1OOg的氯化钠与碳酸钠的饱和溶液,从30℃降至O℃,析出晶体的质量相等 C.t2对应的温度在2O℃-30℃之间
D.欲从含有少量NaCl杂质的碳酸钠浓溶液中分离出碳酸钠晶体,应采取降低溶液温度的方式.
(1)①t1℃时,NaCl的溶解度 Na2CO3的溶解度.(用“>”“<”或“=”表达)
②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度降低而 (填“增大”“减小”或“不变”).“捞碱”后剩余的溶液一定是Na2CO3的 (填“饱和”或“不饱和”)溶液.
③“夏天晒盐”是利用 (填序号)的方法,使NaCl晶体析出.
A.利用风吹日晒,使溶剂蒸发 B.升高温度,使NaCl溶解度增大
(2)根据下表分析:
| 温度 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2CO3 | 7.0 | 12.5 | 21.5 | 39.0 | 49.0 |
②下列几种说法中,正确的是 .
A.碳酸钠晶体的溶解度受温度影响较大
B.将含水各1OOg的氯化钠与碳酸钠的饱和溶液,从30℃降至O℃,析出晶体的质量相等 C.t2对应的温度在2O℃-30℃之间
D.欲从含有少量NaCl杂质的碳酸钠浓溶液中分离出碳酸钠晶体,应采取降低溶液温度的方式.

 (2007?湘潭)在我国某地区有一种“冬天捞碱,夏天晒盐”的说法.这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中含有少量的NaCl.
(2007?湘潭)在我国某地区有一种“冬天捞碱,夏天晒盐”的说法.这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中含有少量的NaCl.