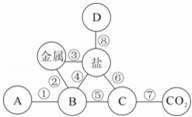
一包白色粉末,由CuSO4、BaCl2、NaOH、NaCl、Na2CO3中的两种或两种以上的物质混合而成.为探究其组成,进行如下实验(假设所有反应均恰好完全):
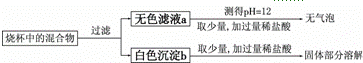
(1)取少量白色粉末,向其中加入足量的水,充分搅拌,固体完全溶解得无色澄清溶液.则原白色粉末中一定不含有 .
(2)取实验(1)所得溶液,加足量的盐酸,产生气泡.则原白色粉末中一定不含有 .
(3)为进一步探究原白色粉末的组成,某同学进行如下实验:
| 实验步骤 | 实验现象 |
| (1)取少量该白色粉末于试管中,加适量的水全部溶解,向溶液中滴加过量的Ba(NO3)2溶液,目的是. |
|
| (2)另取一洁净的试管,取步骤(1)试管中的少量上层清液少许,滴加 . | 溶液变红 |
| (3)另取一洁净的试管,取步骤(1)试管中少量上层清液,滴加 和 溶液. | 出现白色沉淀 |
实验结论
原白色粉末中的定含有 .(写化学式)
同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
推理假设
上述两种物质发生反应的化学方程式为 ,由此推测出废液中一定有NaCl,可能有Na2CO3或HCl
实验探究
(一)确定废液中是否含有盐酸
(1)选择试剂:根据盐酸的化学性质,同学们可选用石蕊、Mg、 、 、 (不同类别的化合物).
(2)实验验证:某同学向废液中加入少量的镁粉,观察到废液中 ,确定一定没有盐酸.
(二)确定废液中是否含有Na2CO3
某同学选用 测出废液的pH=l0,确定废液中一定含有Na2CO3.
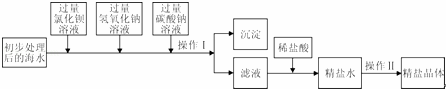
(三)处理废液,回收利用
欲从废液中得到纯净的NaCl,请完成对下列实验方案设计的评价.
| 方案 | 加入试剂 | 分离方法 | 方案评价 (行或不行,并说明理由) |
| 一 | 适量Ca(NO3)2溶液 | 过滤、蒸发结晶 |
|
| 二 | 过量的HCl溶液 | 蒸发结晶 |
|