某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,俊充分反应,实验数据如下:
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
(1)黄铜样品中锌的质量分数为多少?(写出计算步骤,下同)
(2)所用稀硫酸的质量分数为多少?
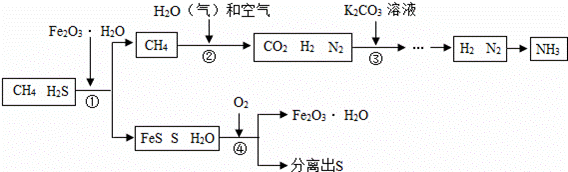
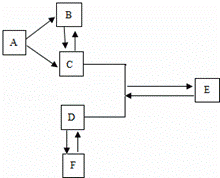
下图是提纯CO、CO2混合气体中的CO并还原氧化铁的示意图.请回答有关问题:

(1)为避免一氧化碳污染空气,并回收利用一氧化碳,方框中连接的是D和E,导管接口的连接顺序为a→ → → e .D装置中NaOH的作用是 .
如果导管连接错误,后果是 .
(2)实验进行一段时间后,B装置的玻璃管中的现象为 ,反应方程式为 .用这种方法“炼”得的铁与工业上炼出的生铁在组成上的最大区别是 .
(3)实验结束后,要从A装置的混合溶液中回收得到较纯净的NaOH固体.
资料显示,在不同温度下NaOH的溶解度如下:
| 温度(℃) | 10 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g/100g水) | 64 | 85 | 138 | 203 | 285 | 376 |
利用实验室的试剂和条件,实验步骤如下(其中Ⅰ、Ⅱ、Ⅲ为实验操作):
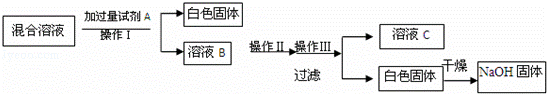
请具体填写试剂A的化学式以及实验操作Ⅰ、Ⅱ、Ⅲ的名称.
①化学式:A ;
②操作名称:Ⅰ Ⅱ Ⅲ .
③如果在操作Ⅱ的过程中,溶液B中出现少量浑浊,原因可能是 .
同学们在实验室进行“粗盐中难溶性杂质的去除”实验.以下是小丽同学的实验报告部分内容.
【实验目的】粗盐中难溶性杂质的去除
【实验过程】
①用托盘天平称取5.0g粗盐,并全部加入到盛有10mL水的烧杯里,边加边用玻璃棒搅拌;
②过滤食盐水,观察滤液无色透明;
③将所得澄清滤液倒入蒸发皿,加热,并用玻璃棒不断搅拌,当液体蒸干时,停止加热;
④用玻璃棒把固体转移到纸上,称量,计算所得精盐的产率.
【实验分析】
(1)步骤①中因为 ,导致实验后精盐产率比其他同学偏低.
(2)步骤③中出现的错误操作是
该操作中玻璃棒的作用
A.加快蒸发速率 B.防止因局部温度过高,造成液滴飞溅 C.引流
【实验反思】经过这样操作所得到的精盐是纯净物吗?
【查阅教材】粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等).
【实验设计】
| 实验操作 | 预计实验现象 | 实验结论及解释 |
| ①将少量所得精盐溶于水,滴加少量稀NaOH溶液 |
| 所得精盐中可能含有氯化镁 化学方程式 |
| ②取实验①中的上层清液继续滴加NaOH溶液至不再有沉淀时,在上层清液中再滴加 碳酸钠(Na2CO3) 溶液 | 出现白色沉淀 | 所得精盐中可能含有氯化钙 化学方程式 |
【实验结论】除去难溶性杂质得到的精盐不是纯净物.
下表列出了2012年颁布的环境空气污染物基本项目浓度限值和2013年4月3日17:00时南京市的空气质量数据监测结果.
| 空气质量等级 | SO2 (1小时平均) | NO2 (1小时平均) | CO (1小时平均) | O3 (1小时平均) | PM2.5 (24小时平均) | PM10 (24小时平均) |
| 一级 | 150 | 200 | 10 | 160 | 35 | 50 |
| 二级 | 500 | 200 | 10 | 200 | 75 | 150 |
| 4月3日南京 实时监测数据 | 38 | 50 | 0.792 | 111 | 57 | 122 |
(数据单位μg/m3,CO为mg/m3)请分析数据并回答问题:
(1)4月3日南京空气质量等级未到达一级,原因是空气中 含量较多.为改善南京空气质量,迎接青奥,下列建议不合理的是 (填序号)
A.采取合理措施,减少建筑工地扬尘 B.植树造林,减少土地裸露面积
C.减少或禁止周边农村燃烧秸杆 D.关闭南京郊区所有化工厂
(2)下列关于空气中污染物的说法正确的是 (填序号)
A.上述四种气体均属于氧化物
B.pH小于7的雨水称为酸雨,SO2、NO2是形成酸雨的主要污染物.
C.大量燃放烟花爆竹会增加空气的污染程度
D.O3含量过大会引起温室效应.