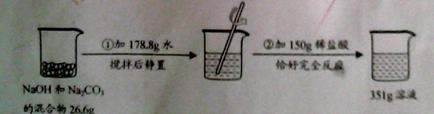
盐城盛产的松花蛋,又称皮蛋、变蛋。其中一种加工工艺的主要原料配方为:鸭蛋10Kg,水10Kg,生石灰1.2Kg,纯碱0.53Kg,食盐0.35Kg。加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍。
请回答下列问题:
(1)鸭蛋中富含的营养素有水和 。
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是 。
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为 色
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动。
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaOH、NaCl
②可能还含有其它溶质
甲同学推断只有Ca(OH)2
乙同学推断只有Na2CO3
丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是 ▲ (用化学方程式表示)。
【实验探究】
| 实验步骤 | 实验现象 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 |
| 另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
【探究结论】 同学的推断是正确的。
【知识应用】①皮蛋食用时加入一些食醋,可以去除氨味和涩感,原因是 。
②料液中起主要作用的是烧碱。现行配方中,直接用烧碱代替石灰和纯碱作用生成的烧碱。若加工10Kg的鸭蛋,需要烧碱的质量是多少千克?(请写出计算过程)
我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献。用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验。
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应。
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳。
[方案一] 样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液。 | 产生白色沉淀 | 反应的化学方程式:
|
(2)分析滴加的CaCl2溶液要过量的原因:___________________;
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量。利用沉淀物质量计算Na2CO3的质量分数为91%。如果不洗涤沉淀物会造成测定结果大于91%,这是因为 _____ 。
[方案二] 样品与稀盐酸反应,测定Na2CO3的质量分数
 利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的)。
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的)。
(4) 打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的 ,再接上装置C和D。
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为__________________ 。
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿。根据 _______________ 定律,装置_________(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数。若没有装置D,将会使测定结果 ________(选填“偏大”或“偏小”)。
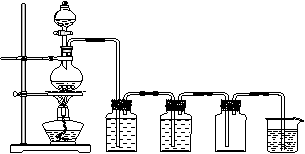
氯气(Cl2)是黄绿色气体,氯气溶于水部分以Cl2分子存在于溶液中,部分与水反应Cl2+H2O=HCl+HClO。产物中,次氯酸HClO是一种弱酸。氯气溶于水所得溶液称为氯水。把品红试纸(染有品 红颜料的滤纸)放入氯水中,品红试纸褪色。下图是实验室制取氯气的成套装置图,请填空:
红颜料的滤纸)放入氯水中,品红试纸褪色。下图是实验室制取氯气的成套装置图,请填空:
| |
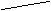
|

|


|

|
⑴仪器X的名称是: 。
⑵从反应物的状态和反应条件看,装置甲属于 型气体发生装置。
⑶氯气在装置丁中被收集,其收集方法为 ,装置戊中可得到氯水。
⑷晓红对“氯水使品红试纸褪色”产生兴趣,她所在的学习小组进行了如下探究,请你
一起来完成:
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜 想】猜想1:氯水中的水使品红试纸褪色;猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;猜想4:氯水中的 (填化学式)使
 品红试纸褪色。
品红试纸褪色。
【实验探究】
| 实 验 操 | 实 验 现 象 | 结 论 |
| ①把品红试纸放入水中 | (A) | 猜想1不成立 |
| ②把品红试纸放入干燥的氯气中 | 试纸不褪色 | 猜想2不成立 |
| ③ | 试纸不褪色 | 猜想3不成立 |
【结 论】学习小组通过讨论,找到了氯水中使品红试纸褪色的物质。
【反 思】向氯水中滴加几滴紫色石蕊试液,会观察到的现象是 。

 作
作