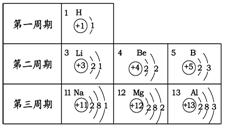
下图是元素周期表中1—18号元素的原子结构示
意图,观察下图,探究下列问题:


(1)核外电子是 排布的。第一层电子数不超过 个;第二层电子数不超过 个;最外层电子数不超过 个。
(2)周期数== 。同一周期的元素,① 相同;
② 逐渐递增;③每周期开头的是 类型的元素,靠近尾部的是 类型的元素,结尾的是 类型的元素。
(3)族数== 。同族元素,① 相同;
② 相似;③ 逐渐递增。
(4)填充下表:
| 元素种类 | 举 例 | 原子的最外层电子数 | 得失电子的趋势 | 元素的化学性质 |
| ①金属元素 | Na、Mg、Al | |||
| ②非金属元素 | O、Cl、S、P | |||
| ③稀有气体元素 | He、Ne、Ar |
(5)最外层为 个电子(只有1个电子层时 个)的结构称为稳定结构。在化学反应中,元素的原子通过得或失电子形成相对稳定结构。
结论:元素的化学性质与 ,特别是 有密切的关系。即 决定元素的化学性质。
元素周期表是学习化学的重要工具,依据下表回答问题:

|
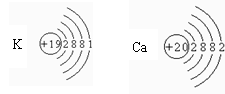
⑵从每一纵行分析,我发现的规律有 。
⑶K、Ca、Mg三种金属单质的失电子能力逐渐减弱,请根据这三种金属元素的原子结构推测:金属单质失电子能力的强弱主要与哪些因素有关?
(任答一条)
在宏观、微观和符号之间建立联系是化学学科的特点。
(1)保持氮气化学性质的最小粒子是 。
(2)右图是钠元素和氯元素在元素周期表中的信息。由此信息得出钠原子的相对原子质量是 ;氯原子的核外电子数是_ ____;钠元素与氯元素最本 质的区别是 __ 不同。
质的区别是 __ 不同。
(3)A、B、C、D表示4种物质,部分物质的微观示意图见下表。
| 物质 |
| C | D | 氢原子 氧原子 碳原子 |
| 微观示意图 |
则B、C、D三种物质的化学符号是 。
 慢熔化
慢熔化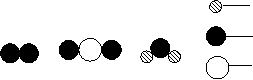 B
B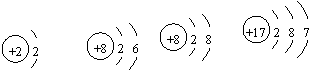 (1)下列示意图表示的粒子中,属于同种元素的是_____(填字母序号)。
(1)下列示意图表示的粒子中,属于同种元素的是_____(填字母序号)。  D
D A.碳元素属于非金属元素
A.碳元素属于非金属元素 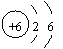 B.碳原子核内质子数为6
B.碳原子核内质子数为6